
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
①pH=7的溶液中:Fe3+、Cl-、Na+、NO3-
②pH=11的溶液中:CO32-、Na+、NO3-、S2-、K+
③水电离的H+浓度为10-12 molL-1的溶液中:NH4+、Na+、SO42-、HCO3-
④加入Mg能放出H2的溶液中:Mg2+、NO3-、NH4+、K+、S2O32-
⑤澄清溶液中:Na+、HCO3-、K+、AlO2-、SO42-
⑥![]() =1×10-12的溶液中:K+、Na+、CO32-、NO3-
=1×10-12的溶液中:K+、Na+、CO32-、NO3-
⑦水溶液中:K+、SO42-、NH4+、NO3-、HCO3-
A.①③⑤⑦B.①④⑤⑥C.②④⑤⑥D.②⑥⑦
【答案】D
【解析】
①Fe3+不会在pH=7的溶液中大量存在,在pH为4.4左右就沉淀完全,故①错误;
②pH=11的溶液呈碱性,CO32-、Na+、NO3-、S2-、K+之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故②正确;
③水电离的H+浓度为10-12molL-1的溶液呈酸性或碱性,HCO3-与氢离子、氢氧根离子都能反应,在溶液中一定不能大量共存,故③错误;
④加入Mg能放出H2的溶液呈酸性,NO3-在酸性条件下具有强氧化性,与Mg反应不会生成氢气,故④错误;
⑤HCO3-能够与AlO2-发生复分解反应生成氢氧化铝沉淀,不能大量共存,故⑤错误;
⑥![]() =1×10-12的溶液显碱性,存在大量氢氧根离子,K+、Na+、CO32-、NO3-之间不反应,都不与氢氧根离子反应,在碱性溶液中能够大量共存,故⑥正确;
=1×10-12的溶液显碱性,存在大量氢氧根离子,K+、Na+、CO32-、NO3-之间不反应,都不与氢氧根离子反应,在碱性溶液中能够大量共存,故⑥正确;
⑦K+、SO42-、NH4+、NO3-、HCO3-之间不反应,在溶液中能够大量共存,故⑦正确;
能够大量共存的为②⑥⑦,故选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是
A. 3g 3He含有的中子数为1NA
B. 1 L 0.1 mol·L1磷酸钠溶液含有的![]() 数目为0.1NA
数目为0.1NA
C. 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D. 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4===ZnSO4+H2↑,下列叙述正确的是( )

A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则锌作正极
D. 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国Lawrece Liermore国家实验室(LINL)成功地在高压下将![]() 转化为具有类似
转化为具有类似![]() 结构的原子晶体,下列关于
结构的原子晶体,下列关于![]() 的原子晶体说法,正确的是:
的原子晶体说法,正确的是:
A. ![]() 的原子晶体和分子晶体互为同分异构体
的原子晶体和分子晶体互为同分异构体
B. 在一定条件下,![]() 原子晶体转化为
原子晶体转化为![]() 分子晶体是物理变化
分子晶体是物理变化
C. ![]() 的原子晶体和
的原子晶体和![]() 分子晶体具有相同的物理性质和化学性质
分子晶体具有相同的物理性质和化学性质
D. 在![]() 的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标号)。
A.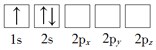 B.
B.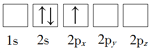
C.![]() D.
D.![]()
(2)Li+与H具有相同的电子构型,r(Li+)小于r(H),原因是______。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是______、中心原子的杂化形式为______。LiAlH4中,存在_____(填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图(a)的BornHaber循环计算得到。
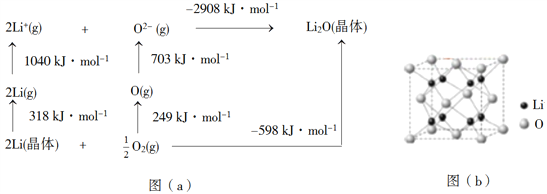
可知,Li原子的第一电离能为________kJ·mol1,O=O键键能为______kJ·mol1,Li2O晶格能为______kJ·mol1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为______g·cm3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸(![]() )常用于制取香精香料。
)常用于制取香精香料。
(1)肉桂酸的分子式是____,肉桂酸____(填“属于”或“不属于”)烃类。
(2)肉桂酸能使溴的四氯化碳溶液褪色,因为结构中含____(填官能团名称)。
(3)向肉桂酸溶液中滴加NaHCO3溶液,实验现象为____。
(4)写出肉桂酸与乙醇发生酯化反应的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验:

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整_________。
(2)实验中他们取6.4 g铜片和12 mL 18 mol·L1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式:__________________;
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是__________________;
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是________(填编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)装置C中试管D内盛装的是品红溶液,当B中气体收集满后,有可能观察到的现象是_____________,待反应结束后,向C中烧杯内加入沸水,D中观察到的现象是_____________。
(4)实验装置C有可能造成环境污染,试用最简单的方法加以解决,__________________(实验用品自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:2SO2+O2![]() 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
编号 | 改变的条件 | 生成SO3速率 |
① | 升高温度 | ________ |
② | 降低温度 | ________ |
③ | 增大氧气浓度 | ________ |
④ | 使用催化剂 | ________ |
⑤ | 压缩体积 | ________ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com