
【题目】碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容。
(1)已知热化学方程式:
①2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH1
②C(s)+O2(g)===CO2(g) ΔH2
③H2(g)+1/2O2(g)===H2O(l) ΔH3
则反应④2C(s)+H2(g)===C2H2(g)的ΔH=_________。(用含ΔH1、ΔH2、ΔH3的关系式表示)
(2)利用上述反应①设计燃料电池(电解质溶液为氢氧化钾溶液),写出电池的负极反应式:___________。
(3)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g) ΔH<0。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) ΔH<0。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间/min 浓度/(mol·L-1) 物质 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①1~10 min内,NO的平均反应速率
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________(填字母编号)。
a.通入一定量的NO
b.加入一定量的C
c.适当升高反应体系的温度
d.加入合适的催化剂
e.适当缩小容器的体积
【答案】2ΔH2+ΔH3-ΔH1/2 C2H2-10e-+14OH-==2CO32—+8H2O 0.042 mol·L-1·min-1 9/16 < ae
【解析】
(1)根据盖斯定律进行计算;
(2)原电池负极发生氧化反应,电解质溶液为氢氧化钾溶液,C2H2放电生成2CO32-,利用C元素化合价变化判断失去电子数,根据电荷守恒和质量守恒写出电极反应式;
(3)①计算0min~10min内,NO浓度的变化,得到v(NO);20min后达到化学平衡状态,利用化学平衡常数表达式计算,化学平衡常数;
②利用化学平衡状态的特征判断。
(1)已知热化学方程式:①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH1;②C(s)+O2(g)=CO2(g) ΔH2;③H2(g)+1/2O2(g)=H2O(l) ΔH3;则根据盖斯定律可知②×2+③-①×1/2即可得到反应④2C(s)+H2(g)=C2H2(g)的ΔH=2ΔH2+ΔH3-1/2ΔH1,故答案为:2ΔH2+ΔH3-1/2ΔH1。
(2)原电池负极发生氧化反应,电解质溶液为氢氧化钾溶液,C2H2放电生成2CO32-,C元素化合价升高了5,即1molC2H2失去10mole-,电极反应式为:C2H2-10e-+14OH-=2CO32-+8H2O,故答案为:C2H2-10e-+14OH-=2CO32-+8H2O。
(3)①0min~10min内,NO浓度的变化为1.00mol/L-0.58mol/L=0.42mol/L,v(NO)=0.42mol/L÷10min=0.042mol·L-1·min-1,
根据题意和表中数据,20min~30min,40min~50min都是T1℃时的化学平衡,20℃反应达到平衡状态,平衡浓度c(NO)=0.40mol/L,c(N2)=0.3mol/L,c(CO2)=0.30mol/L,C(s)+2NO(g)═N2(g)+CO2(g),平衡常数K1=0.30×0.30/0.402=9/16;
应正反应ΔH<0,温度由T1℃降至T2℃,化学平衡右移,K值增大,所以K1<K2;
故答案为:0.042mol·L-1·min-1;9/16;<。
②30min后,只改变某一条件,反应重新达到平衡,图表数据分析可知一氧化氮,氮气,二氧化碳浓度都增大;
a.通入一定量的NO,反应正向进行,达到平衡后一氧化氮、氮气、二氧化碳浓度增大,故a符合;
b.加入一定量的活性炭是固体,对平衡无影响,故b不符合;
c.升高体系的温度,会使平衡左移,NO浓度增大,而N2、CO2浓度减小,故c不符合;
d.加入合适的催化剂,只能改变化学反应速率,不能改变平衡,浓度不变,故d不符合;
e.适当缩小容器的体积,反应前后是气体体积不变的反应,平衡不动,但个物质浓度增大,符合要求,故e符合。
故答案为:ae。


科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间有如下转化关系: 下列有关物质的推断不正确的是 ( )
下列有关物质的推断不正确的是 ( )
A. 若甲为AlC13溶液,则丁可能是NaOH溶液 B. 若甲为N2,则丁可能是O2
C. 若甲为Fe,则丁可能是稀硝酸 D. 若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是一种具有应用前景的绿色电源。下图为燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:
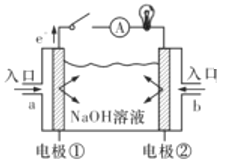
(1)若该燃料电池为氢氧燃料电池。
①a极通入的物质为_____(填物质名称),电解质溶液中的OH—移向______极(填”负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:______________。
(2)若该燃料电池为甲烷燃料电池。已知电池的总反应为CH4+2O2+2OH-=CO32-+3H2O
①下列有关说法正确的是___________(填字母代号)。
A.燃料电池将电能转变为化学能
B.负极的电极反应式为CH4+10OH--8e-=CO32-+7H2O
C.正极的电极反应式为O2+4H++4e-=2H2O
D.通入甲烷的电极发生还原反应
②当消耗甲烷33.6L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子的物质的量为______mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处于平衡状态的反应2 H2 S(g) ![]() 2H2(g)+S2(g)
2H2(g)+S2(g) ![]() H>0,不改变其他条件的情况下合理的说法是
H>0,不改变其他条件的情况下合理的说法是
A.加入催化剂,反应途径将发生改变,![]() H也将随之改变
H也将随之改变
B.升高温度,正逆反应速率都增大,H2S分解率也增大
C.增大压强,平衡向逆反应方向移动,将引起体系温度降低
D.若体系恒容,注人一些H2后达新平衡,H2浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过图像分析影响化学平衡移动的因素,某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g) 2SO3(g) ΔH<0的正、逆反应速率的影响如图所示:

①加催化剂对反应速率影响的图像是___(填字母,下同),平衡____移动。
②升高温度对反应速率影响的图像是___,平衡向____方向(填“正反应”或“逆反应”,下同)移动。
③增大反应容器体积对反应速率影响的图像是___,平衡向____方向移动。
④增大O2的浓度对反应速率影响的图像是___,平衡向____方向移动。
⑤上述①到④中的外界条件,使得单位体积内活化分子百分数增大的是___(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为某种乙醇燃料电池示意图,工作时电子流方向如图所示,下列判断正确的是

A.X为氧气
B.电极A反应式:CH3CH2OH-12e-+3H2O=2CO2+12H+
C.电极材料活泼性:A>B
D.B电极附近溶液pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有①16O、17O、18O ②H2、D2、T2 ③石墨、金刚石 ④1H、2H、3H四组微粒或物质。互为同位素的是(填序号)___________;互为同素异形体的是(填序号)____________;由①和④的微粒可组成____________种不同的三原子化合物。
(2)用电子式表示下列过程:
①MgCl2的形成过程 ________________;
②H2S的形成过程_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①NaCl、②干冰、③冰、④Na2O2、⑤白磷(P4)、⑥金刚石、⑦Na2CO3、⑧钠。以上物质中属于离子晶体的是____________;属于分子晶体的是____________(填序号)。氯化钡是无色晶体,溶于水,水溶液能导电,熔点1 560 ℃。它可能属于____________晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时在10 mL 0.1mol·L—1Na2CO3溶液中逐滴加入0.1 mol·L—1HCl溶液20 mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示。下列说法正确的是( )

A. 0.1 mol·L—1Na2CO3溶液中c(Na+)+c(H+)=c(OH—)+c(CO32—)+c(HCO3—)
B. 当加入10mL盐酸时,所得混合溶液pH>7
C. 当pH=8时,c(Na+)=c(CO32—)+c(HCO3—)+c(H2CO3)
D. 在M点:c(CO32—)=c(HCO3—)>c(Na+)>c(OH—)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com