
| A. | C4H8 | B. | C5H12O | C. | C5H11Br | D. | 酯C5H10O2 |
分析 (A)根据C4H8属于烯烃和环烷烃的种类分析;
(B)分子式为C5H11OH,分析饱和一元醇、饱和一元醚的种数;
(C)根据C5H12的等效氢有多少种,它的一溴代物就有多少种进行分析;
(D)分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,进行判断.
解答 解:(A)C4H8属于烯烃的同分异构体有3种,属于环烷烃的有2种,共5种;
(B)改写成C5H11OH,C5H11-是戊基,有8种,所以饱和一元醇有8种,饱和一元醚可写成C4H9-O-CH3,C4H9-是丁基,有4种,饱和一元醚还可写成C3H7-,丙基有2种,所以饱和一元醚共有6种,C5H11OH的同分异构体共有14种;
(C)C5H11Br,C5H12的等效氢有8种,所以C5H11Br同分异构体有8种;
(D)若为甲酸和丁醇酯化,丁醇有4种,形成的酯有四个:
HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3;
若为乙酸和丙醇酯化,丙醇有2种,形成的酯有2个:CH3COOCH2CH2CH3、CH3COOCH(CH3)2;
若为丙酸和乙醇酯化,丙酸有1种,形成的酯有1个:CH3CH2COOCH2CH3;
若为丁酸和甲醇酯化,丁酸有2中,形成的酯有2个:CH3CH2CH2COOCH3、(CH3)2CHCOOCH3,共有9种;
故选B.
点评 本题考查有机物的推断、同分异构体的书写,难度中等,注意确定的方法.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:选择题

| A. | 丙中一定含有羧基 | B. | 甲不可以与HBr发生取代反应 | ||
| C. | 甲、乙、丙都能发生氧化反应 | D. | 可以用溴水检验乙中的碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
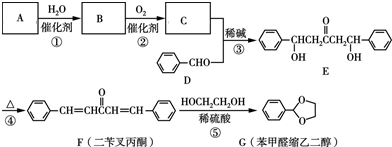
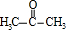 +2
+2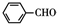 $\stackrel{碱}{→}$
$\stackrel{碱}{→}$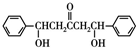 .
.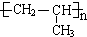 .
.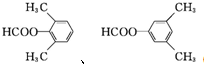 .
.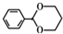 (无机物任选).
(无机物任选).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
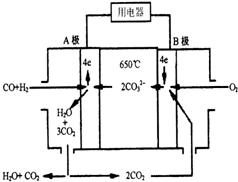 现有一个碳酸盐燃料电池,以一定比例的Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,直接以水煤气(CO、H2的体积比为1:1)为燃料,其工作原理如图所示.
现有一个碳酸盐燃料电池,以一定比例的Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,直接以水煤气(CO、H2的体积比为1:1)为燃料,其工作原理如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 石油的分馏、煤的干馏均是物理变化 | |
| B. | 应当大力实施矿物燃料“脱硫“、脱硝技术”,减少硫的氧化物和氮氧化物的污染 | |
| C. | 近期我国华北地区出现雾霸天气,PM2.5超标.PM2.5仅来自煤的燃烧 | |
| D. | 根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等浓度的①(NH4)2SO4溶液、②NH4HCO3溶液、③NH4Cl溶液中的c(NH4+):①>③>② | |
| B. | 等体积pH=a的醋酸与pH=b的NaOH溶液(a+b=14)充分混合时,可能有:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 已知Ka(HClO)=3.0×10-8,Ka(HCN)=6.2×10-10,等体积、等浓度的NaClO、NaCN溶液中,前者中的离子总数小于后者中的离子总数 | |
| D. | 向20mL氨水中加入10mL等浓度的盐酸,有c(NH4+)-c(NH3•H2O)=2[c(OH-)-c(H+)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在中和滴定实验中,锥形瓶须用待测液润洗 | |
| B. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| C. | 用标准盐酸溶液滴定未知浓度NaOH溶液时,若滴定前滴定管尖嘴处有气泡未排出而滴定后消失,则能使所测结果偏高 | |
| D. | 滴定时可将KMnO4溶液装在碱式滴定管中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
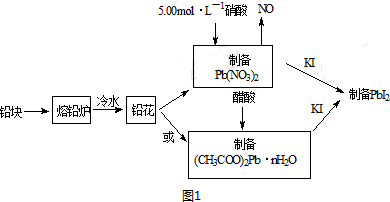
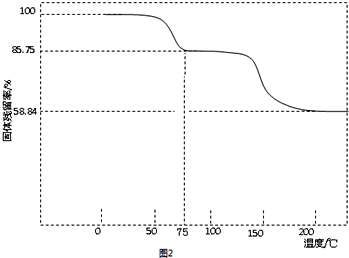
| 实验内容 | 实验方法 | 实验现象及原因分析 |
| ①碘离子浓度增大对平衡的影响 | 取PbI2饱和溶液少量于一支试管中,再滴入几滴NaI饱和溶液 | 现象:溶液中c(I-)增大,使Q大于了PbI2的Ksp |
| ②铅离子浓度减小对平衡的影响 | 取PbI2悬浊液少量于一支试管中,再加入少量NaCl饱和溶液 | 现象:黄色浑浊消失 原因:形成PbCl42-,导致溶液中c(Pb2+)减小,使Qc小于PbI2的Ksp |
| ③铅离子和碘离子浓度都减小对平衡的影响 | 在PbI2悬浊液中滴入几滴FeCl3饱和溶液 | 现象:黄色浑浊消失 写出反应的离子方程式:PbI2+2Fe3++4Cl-=PbCl42-+2Fe2++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com