


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
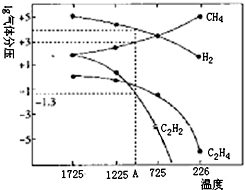 ��Ȳ��C2H2��������������л��ϳ�����;�dz��㷺�����ɵ�ʯ��CaC2��ֱ��ˮ�����������1500�����������ѽⷨ������
��Ȳ��C2H2��������������л��ϳ�����;�dz��㷺�����ɵ�ʯ��CaC2��ֱ��ˮ�����������1500�����������ѽⷨ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ԭ�Ӱ뾶��Na��Mg |
| B�����ԣ�NaOH��KOH |
| C�����H+��������CO32-��Cl- |
| D����ԭ�ԣ�I-��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��p2��p1��Q��0 |
| B��p2��p1��Q��0 |
| C��p2��p1��Q��0 |
| D��p2��p1��Q��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
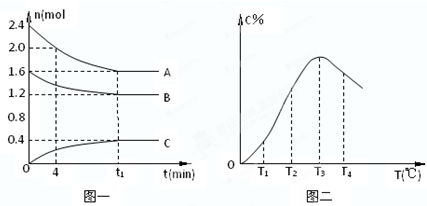
| A��0��4����ʱ��A������Ϊ0.01mol/��L?min�� | ||
| B����T1��T2�仯ʱ��V����V | ||
C���÷�Ӧ��ƽ�ⳣ������ʽK=
| ||
| D���˷�Ӧ������ӦΪ���ȷ�Ӧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2O2��Na2O�� |
| B��KCl��KClO3�� |
| C��Na2CO3��NaHCO3�� |
| D��NH4Cl��I2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com