
����Ŀ��ij�о���ѧϰС����̽��FeSO4��7H2O���̷�������Ҫ��ѧ���ʺ���;��
I��FeSO4��7H2O���̷����㷺����ҽҩ��ҵ����������FeSO4��7H2O��ʵ�����Ʊ�����ͼ��
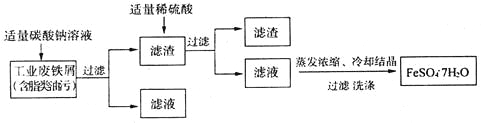
��������ش��������⣺
��1��̼������Һ�ܳ�ȥ֬����������Ϊ_________________���ñ�Ҫ������˵������
��2������м�к���������Fe2O3�����Ʊ������������ȥ��������___________________���ñ�Ҫ�����ӷ���ʽ˵������
II��Ϊ�ⶨij��Ѫ������Ч�ɷ�ΪFeSO4��7H2O������Ԫ�غ��������ʵ���������£��ش��������⣺
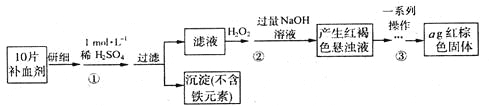
��1����������Ҫ��Ũ���ᣨ��������Ϊ98.3 %������100 mL 1 mol��L-1��ϡ���ᣬ���õIJ�����������Ͳ���ձ�������������ͷ�ιܼ�____________��
��2������������ʾ��һϵ�в��������ǣ�
a������
b.ϴ��
c��__________
d����ȴ
e������
f���ظ�c��eֱ��������������
����f��Ŀ����_________________________________________________________��
��3������ʵ���������Ԫ������ģ���ÿƬ��Ѫ������Ԫ��Ϊ________g���ú�n�Ĵ���ʽ��ʾ����
III��������ͼװ��̽���̷������ȶ���
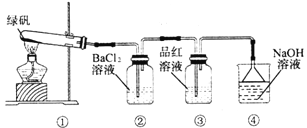
��1��ʵ������У��۲쵽����Ʒ����Һ��ɫ���ݴ��Ʋ�FeSO4�ֽ���������п��ܱ�������Ԫ����___________����д�����з�Ӧ�����ӷ���ʽ��____________________��
��2�������а�ɫ�������ɣ�С���Ա�������۷�������ϣ�1���еı����Ʋ⣬�̷��ֽ�IJ������п��������и����е�______________���������ĸ����
a��Fe2O3��SO3��H2O
b��Fe2O3��SO2��SO3��H2O
c��FeO��SO2��SO3��H2O
���𰸡�̼���ˮ��ʼ��ԣ��ڼ�����������֬��ˮ������������ˮ�����ʶ�����ȥ Fe2O3+6H+=2Fe3++3H2O��2Fe3++Fe=3Fe2+�� Fe2O3+Fe+ 6H+=3Fe2++3H2O 100mL����ƿ ���գ����ȣ� ʹ����������ȫ�ֽ����������� 0.07a Fe 2OH-+ SO2= SO32-+H2O ��OH-+ SO2= HSO3- b
��������
����м�к����������ۣ�Na2CO3Ϊǿ�������Σ�CO32-ˮ������HCO3-��OH-�����ߴٽ�CO32-ˮ�⣬��ٽ���֬ˮ�⣬Ȼ�����ϴ�ӣ�����ϡ���ᣬ������ӦIIΪFe+H2SO4=FeSO4+H2�������ȹ��ˡ���ȴ�ᾧ������ϴ�ӵõ�FeSO47H2O��
����Ѫ����ϸ����ҩƬ�м���ϡ���ᣬȻ����˵õ�����������Һ�м���˫��ˮ��������Ӧ2Fe2++H2O2+2H+=2Fe3++2H2O������Һ�м������X��Һ���ɺ��ɫ��������XΪ������ɫ�������յõ�����ɫ����Fe2O3���ݴ˷������
���̷����������Ӿ��л�ԭ�ԣ�����β������װ�ã�����������NaOH��Һ��Ӧ���ݷ�Ӧ�����֪���̷��ֽ������˶���������������������ԭ��Ӧ�л��ϼ��н������������������������ɡ�
I����1��̼������Һ�ܳ�ȥ������������Ϊ̼���ˮ��ʼ��ԣ��ڼ�����������֬��ˮ������������ˮ�����ʶ�����ȥ��
��2�����˺�õ���������Fe2O3��Fe�Ļ������������ᷢ����Ӧ��Fe2O3������ᷴӦ�����ɵ�Fe3+�������Ӧ����ȥ������Fe2O3���ó�ȥ����Ӧ���ӷ���ʽ�У�Fe2O3+6H+=2Fe3++3H2O��2Fe3++Fe=3Fe2+��
II.��1������һ�����ʵ���Ũ�ȵ���Һһ��Ҫ�õ�����ƿ��ѡ��100mL����ƿ��
��2�����ɵĺ��ɫ������Fe��OH��3������ɫ������Fe2O3��Ҫ��Fe��OH��3,ת��ΪFe2O3��Ҫ���ջ���ȣ��ظ�c��eֱ����������������Ϊ��ʹ����������ȫ�ֽ�������������
��3��Fe2O3������Ϊag�����е���Ԫ������Ϊ��112/160g=0.7a������ÿƬ��Ѫ������Ԫ��Ϊ0.07a g��
III.��1��Ʒ����ɫ˵����SO2���ɣ�SԪ�ػ��ϼ۽��ͣ���ô��Ԫ�ػ��ϼ۾�Ҫ���ߣ����Ա���������Fe Ԫ�� ������NaOH��Һ����SO2����Ӧ�����ӷ���ʽΪ��2OH-+ SO2= SO32-+H2O ��OH-+ SO2= HSO3-��
��2�������а�ɫ������������SO3���ɣ������̷��ֽ�IJ������п�����Fe2O3��SO2��SO3��H2O��ѡb��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�������c(H+)=1��10-12molL-1����Һ�У�һ���ܴ����������������( )
A.NH![]() ��Ba2+��NO
��Ba2+��NO![]() ��Cl-B.Cl-��SO
��Cl-B.Cl-��SO![]() ��Na+��K+
��Na+��K+
C.SO![]() ��NO
��NO![]() ��Fe2+��Mg2+D.Na+��K+��ClO-��I-
��Fe2+��Mg2+D.Na+��K+��ClO-��I-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����п������õİ�ͷ����������H�ĺϳ�·����ͼ��ʾ��
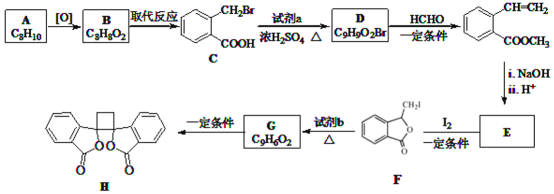
��֪��
![]()
![]() R��HC=CH��R��
R��HC=CH��R��
ii��R��HC=CH��R��![]()
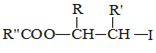
iii��R��HC=CH��R��![]()
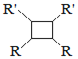
![]() ����R��
����R��![]() ��
��![]() �����⡢�������
�����⡢�������![]()
![]() ���ڷ���������������______��
���ڷ���������������______��
![]() �Ľṹ��ʽ��______��
�Ľṹ��ʽ��______��
![]() ��F����G�ķ�Ӧ������______��
��F����G�ķ�Ӧ������______��
![]() ��E��
��E��![]() ��һ�������·�Ӧ����F�Ļ�ѧ����ʽ��______���˷�Ӧͬʱ��������һ���л�����������F��Ϊͬ���칹�壬���л�������Ľṹ��ʽ��______��
��һ�������·�Ӧ����F�Ļ�ѧ����ʽ��______���˷�Ӧͬʱ��������һ���л�����������F��Ϊͬ���칹�壬���л�������Ľṹ��ʽ��______��
![]() ����˵����ȷ����______
����˵����ȷ����______![]() ѡ����ĸ���
ѡ����ĸ���![]() ��
��
A.G����˳���칹��
B.��G����H�ķ�Ӧ�Ǽӳɷ�Ӧ
C.1molG��������1mol![]() �����ӳɷ�Ӧ
�����ӳɷ�Ӧ
D.1molF��1molH������NaOH��Һ��Ӧ��������2molNaOH
![]() ����ϩΪ��ʼԭ�ϣ������֪��Ϣѡ�ñ�Ҫ�����Լ��ϳ�
����ϩΪ��ʼԭ�ϣ������֪��Ϣѡ�ñ�Ҫ�����Լ��ϳ� ��д���ϳ�·��
��д���ϳ�·��![]() �ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ����
�ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ����![]() ��______��
��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ�����,����˵����ȷ����
A. 124 g P4����P��P���ĸ���Ϊ4NA B. 12 gʯī�к���C��C���ĸ���Ϊ1��5NA
C. 12 g���ʯ�к���C��C���ĸ���Ϊ4NA D. 60gSiO2�к�Si��O���ĸ���Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڹ�ҵ������˵���У�����ȷ����
A. ��ҵ�ϣ��ý�̿�ڵ�¯�л�ԭ��������õ����������ʵĴֹ�
B. �ȼҵ�����õĽ���ĤΪ�����ӽ���Ĥ����������ͨ������ֹ��������Ӧ����������Ʋ�����
C. ������ͨ��������Ҫԭ����ʯ��ʯ��ʯӢ�ʹ���
D. �ڸ�¯�����ķ�Ӧ�У���̿Ϊ����ʯ�Ļ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���¶Ⱥ�ѹǿ�Է�ӦX��Y![]() 2ZӰ���ʾ��ͼ��ͼ�к������ʾ�¶ȣ��������ʾƽ����������Z���������������������ȷ���ǣ� ��
2ZӰ���ʾ��ͼ��ͼ�к������ʾ�¶ȣ��������ʾƽ����������Z���������������������ȷ���ǣ� ��
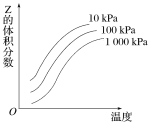
A.�������淴Ӧ������ӦΪ���ȷ�ӦB.X��Y��Z��Ϊ��̬
C.X��Y�����ֻ��һ��Ϊ��̬��ZΪ��̬D.������Ӧ���淴Ӧ����H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4A(s)��3B(g)��2C(g)��D(g)����2 min��B��Ũ�ȼ�����0.6mol/L�����з�Ӧ���ʵı�ʾ��ȷ����
A. ��A��ʾ�ķ�Ӧ������0.4 mol/(L��min)
B. ��C��ʾ�ķ�Ӧ������0.2 mol/(L��min)
C. 2 minĩʱ�ķ�Ӧ���ʣ���B��ʾ��0.3 mol/(L��min)
D. ����2 min����B��ʾ�ķ�Ӧ���ʵ�ֵ�Ǽ�С�ģ�C��ʾ�ķ�Ӧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��ֱ���0.1mol/L��Һ��������ʵ�飬��������ȷ����![]()
![]()
A.��![]() ��Һ��ͨ
��Һ��ͨ![]() ��
��![]() ��c(Na+)��c(HCO3-)+ 2c(CO32-)
��c(Na+)��c(HCO3-)+ 2c(CO32-)
B.��![]() ��Һ�м����Ũ�ȵ���������c(Na+)��c(Cl-)
��Һ�м����Ũ�ȵ���������c(Na+)��c(Cl-)
C.��![]() ��Һ�м����Ũ�ȵ������
��Һ�м����Ũ�ȵ������![]() ��Һ��pH=13
��Һ��pH=13
D.��ˮ�м�������![]() ���壺
���壺![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ȼ�ѧ����ʽSO2(g)+1/2O2(g)![]() SO3(g) ��H=-98.32kJ��mol-1,�������г���2mol SO2��1mol O2��ַ�Ӧ,���շų�������
SO3(g) ��H=-98.32kJ��mol-1,�������г���2mol SO2��1mol O2��ַ�Ӧ,���շų�������
A. ����196.64kJ B. ����196.64kJ��mol-1
C. ��196.64kJ D. ����196.64kJ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com