
 ��2L�ܱ������ڣ�800��ʱ��Ӧ2NO��g��+O2��g��=2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���
��2L�ܱ������ڣ�800��ʱ��Ӧ2NO��g��+O2��g��=2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
���� ��1���ӱ��п�֪5sʱ��һ�����������ʵ���Ϊ0.007mol������һ��������ʼ���ʵ������㣻
��2������һ���������ʵ����ı仯֪��һ�����������ʵ����ڼ��٣���������������ʵ����ڲ���������ͬһʱ����ڣ�һ���������ٵ����ʵ������ڶ����������ӵ����ʵ��������ݡ�v=$\frac{\frac{��n}{V}}{��t}$����һ�������ķ�Ӧ���ʣ��ٽ��ͬһ��ѧ��Ӧͬһʱ����ڣ������ʵķ�Ӧ����֮�ȵ����������֮�ȼ��������ķ�Ӧ���ʣ�
��3�����ݻ�ѧƽ��״̬��������𣬵���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯������ʱҪע�⣬ѡ���жϵ������������ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��
��� �⣺��1���ӱ��п�֪5sʱ��һ�����������ʵ���Ϊ0.007mol��һ��������ʼ���ʵ���Ϊ0.020mol����NO��ת����=$\frac{һ�������仯�����ʵ���}{һ����������ʼ���ʵ���}$��100%=$\frac{0.020mol-0.007mol}{0.020mol}$=65%��
�ʴ�Ϊ��65%��
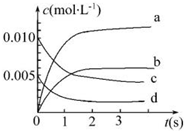
��2������һ���������ʵ����ı仯֪��һ�����������ʵ����ڼ��٣���������������ʵ����ڲ���������ͬһʱ����ڣ�һ���������ٵ����ʵ������ڶ����������ӵ����ʵ�����ͼ������������Ũ�ȣ����Ա�ʾNO2�ı仯��������b��
0��2s��v��NO��=$\frac{0.20mol-0.008mol}{2L}$��2min=0.0030mol/��L��min����ͬһ��ѧ��Ӧͬһʱ����ڣ������ʵķ�Ӧ����֮�ȵ����������֮�ȣ����������ķ�Ӧ����Ϊ 0.0015mol/��L•s����
�ʴ�Ϊ��b��0.0015mol/��L•s����
��3��a�����ж����淴Ӧ�����Ƿ���ȣ���a����
b����Ӧǰ�����������ͬ��ѹǿ����˵�����������ʵ������䣬��������ʵ������䣬�ﵽƽ�⣬��b��ȷ��
c��v����NO��=2v����O2��ʱ��˵�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬����c��ȷ��
d��������������Ӧ�������ﶼ�������������䣬�����ܶ�ʼ�ղ��䣬�ܶȲ���˵����һ���ﵽƽ�⣬��d����
�ʴ�Ϊ��bc��
���� ���⿼���˿��淴Ӧ���жϡ���Ӧ���ʵļ��㡢��ѧƽ��״̬���жϣ�ע��ѹǿ���ܶȲ���ʱƽ��״̬���ж�Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ�͵Ĵ������ǻ�÷���������Ҫ;�� | |
| B�� | 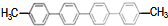 �����ϵ�һ�ȴ�����4�� �����ϵ�һ�ȴ�����4�� | |
| C�� | ȼ�յ������ļ���ͱ�ϩ����ϩ��Ҫ��O2���� | |
| D�� | 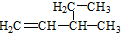 ����Ϊ3-��-1-��ϩ ����Ϊ3-��-1-��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 1 | �� | |||||||
| 2 | �� | �� | �� | �� | ||||
| 3 | �� | �� | �� | �� | �� |
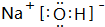 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ǻ�ֱ�������ڱ������Ǵ� | |
| B�� | �ǻ�ֱ�������ڱ�������̼ԭ�����Ǵ������� | |
| C�� | �ǻ�ֱ�������ڱ�������̼ԭ�����Ƿ������� | |
| D�� | �������Ļ����ﲻ���ܼȺ����ǻ��ֺ����ǻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����ô�����̼�����ϡ���ᷴӦ��ȡ������̼���壬��ش�
�����ô�����̼�����ϡ���ᷴӦ��ȡ������̼���壬��ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
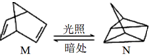 ��H=+88.6kJ/mol
��H=+88.6kJ/mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
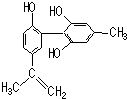 �ҹ�֧�֡����İ��ˡ���һ����Ҫ�����ǣ���������˶�Ա�����˷ܼ���ij���˷ܼ��Ľṹ��ʽ��ͼ��ʾ���йظ����ʵ�˵����ȷ���ǣ�������
�ҹ�֧�֡����İ��ˡ���һ����Ҫ�����ǣ���������˶�Ա�����˷ܼ���ij���˷ܼ��Ľṹ��ʽ��ͼ��ʾ���йظ����ʵ�˵����ȷ���ǣ�������| A�� | ��FeCl3��Һ����ɫ����Ϊ�������뱽������ͬϵ�� | |
| B�� | ����KMnO4��H+����Һ���۲���ɫ��ȥ��˵���ṹ����һ�����ڲ�����̼̼˫�� | |
| C�� | 1 mol�����ʷֱ���Ũ��ˮ��H2��Ӧʱ�������Br2��H2�ֱ�Ϊ4mol��7 mol | |
| D�� | �÷����е�����ԭ���п��ܹ�ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| ���� | Cu | Cu | Zn | Al |
| ���� | Zn | Zn | Cu | Zn |
| �������Һ | H2SO4 | CuSO4 | ZnCl2 | Cu Cl2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��ij�л���A�ķ����У����з��ǻ������ǻ����Ȼ��ȹ����ţ���ṹ��ʽ��ͼ��
��ij�л���A�ķ����У����з��ǻ������ǻ����Ȼ��ȹ����ţ���ṹ��ʽ��ͼ��

 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com