
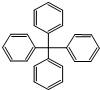
| A. | 分子式为C25H20 | |
| B. | 分子中所有原子有可能处于同一平面 | |
| C. | 该化合物分子中所有原子不可能处于同一平面 | |
| D. | 分子中处于同一平面的原子最多23个 |
分析 有机物具有苯和甲烷的结构特点,苯环所有原子共平面,甲烷具有正面体结构,以此解答该题.
解答 解:A.分子中含有4个苯环,共含有25个C和20个H,则分子式为C25H20,故A正确;
B.分子中含有饱和烃基,具有甲烷的结构特点,所有碳原子不可能在同一平面上,故B错误;
C.甲烷的正四面体结构,烃分子中氢原子被其它原子取代后,其空间位点不变,由于甲烷分子中的四个氢原子位于正四面体的四个顶点上,当4个氢原子全部被苯基取代后,苯基就排在正四面体的四个顶点上,故该化合物分子中所有原子不可能处于同一平面,故C正确;
D.根据三点确定一个平面,有机物中两个苯环、饱和碳原子可能位于同一平面,则原子数最多为23,故D正确.
故选B.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于考查学生的分析能力和综合运用化学知识的能力,注意把握有机物的空间结构,为解答该题的易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 凡是中心原子采取sp3杂化轨道成键的分子立体构型都是正四面体 | |
| B. | CH4中的sp3杂化轨道是4个H原子的1s 轨道和C原子的2p轨道混合形成 | |
| C. | sp3杂化轨道是由同一原子中能量相近的s 和p轨道混合形成的一组新轨道 | |
| D. | 凡AB3型的共价化合物,中心原子A均采用sp3杂化轨道成键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | T、Q、W、Y的原子半径大小为:T<Q<Y<W | |
| B. | Q与W形成的两种常见化合物中含有相同比例的阴、阳离子,属于同种晶体类型 | |
| C. | Q与Y组成的常见物质是一种碱性氧化物 | |
| D. | 由Y和T组成的物质YT是原子晶体,在电子和陶瓷工业上有广泛应用,可以直接由单质Y和T在低温下合成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯和油脂均能发生水解反应生成醇 | |
| B. | 丙烯与氯气只能发生加成反应 | |
| C. | 溴乙烷与氢氧化钠的水溶液可反应生成乙烯 | |
| D. | 苯可以使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
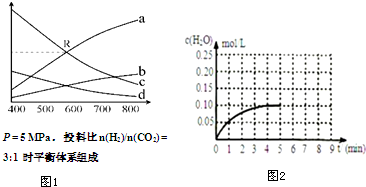
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的中子数 | B. | 13C与C60互为同素异形体 | ||
| C. | 15N与14N互为同位素 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H、D、T表示同一种核素 | B. | F-原子结构示意图: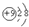 | ||
| C. | 用电子式表示HCl形成过程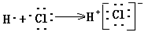 | D. | NaOH既含共价键又含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4固体熔化时破坏的是离子键和共价键 | |
| B. | NaHSO4固体中阳离子和阴离子的个数比是2:1 | |
| C. | NaHSO4固体溶于水时既破坏离子键又破坏共价键 | |
| D. | 因为NaHSO4是离子化合物,因此能够导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 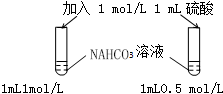 探究浓度对化学反应速率的影响 | B. | 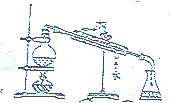 分离乙醇和乙酸的混合溶液 | ||
| C. | 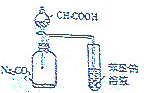 证明酸性:CH3COOH>H2CO3>苯酚 | D. | 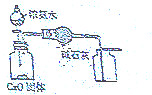 制取并且收集干燥纯净的NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com