
分析 (1)根据n=cV和m=nM来计算;氢氧化钠固体易潮解;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
解答 解:(1)溶液中的氢氧化钠的物质的量n=cV=1mol/L×0.25L=0.25mol,质量m=nM=0.25mol×40g/mol=10.0g;氢氧化钠固体易潮解,故称量的时候要放在烧杯中进行,故答案为:10.0,小烧杯;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器为:250mL容量瓶、烧杯、玻璃棒、胶头滴管和托盘天平,故称量后配制此溶液最主要的仪器名称是250mL容量瓶,故答案为:250mL容量瓶;
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和仪器选择,属于基础型题目,难度不大.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 3:2 | B. | 2:3 | C. | 4:1 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钙和磷都是人体内含量丰富的矿物元素,属于常量元素 | |
| B. | 白色污染是指聚乙烯、聚氯乙烯等各种废塑料制品造成的污染 | |
| C. | 具有强吸附性的活性炭能吸附某些溶于水中的杂质,并能对水进行消毒 | |
| D. | 青霉素等抗生素对某些微生物有抑制或杀灭作用,但对人体细胞的毒性很低 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
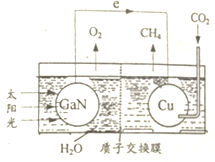 科学家用氮化镓材料与铜组装如图所示人工光合系统,利用该装置成功地实现了以CO2和H20合成CH4.下列有关说法正确的是
科学家用氮化镓材料与铜组装如图所示人工光合系统,利用该装置成功地实现了以CO2和H20合成CH4.下列有关说法正确的是| A. | 该装置中存在两种能量的转换形式 | |
| B. | 电池工作时,H+向负极移动 | |
| C. | 为提高该人工光合系统的工作效率,最好向装置中加入少量盐酸 | |
| D. | 铜电极表面的电极反应式为:C02+8e-+8H+═CH4+2H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
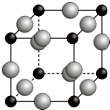 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com