
| A£® | FeCl3 | B£® | CaCl2 | C£® | FeCl2 | D£® | KCl |
·ÖĪö ĀČĘų¾ßÓŠĒæŃõ»ÆŠŌ£¬Óė±ä¼Ū½šŹō·“Ӧɜ³Éøß¼Ū½šŹōĀČ»ÆĪļ£¬ŅŌ“ĖĄ“½ā“š£»
½ā“š ½ā£ŗA£®FeÓėĀČĘų·“Ӧɜ³ÉFeCl3£¬¹ŹA²»Ń”£»
B£®CaÓėĀČĘų·“Ӧɜ³ÉCaCl2£¬¹ŹB²»Ń”£»
C£®FeÓėĀČĘų·“Ӧɜ³ÉFeCl3£¬¹ŹCŃ”£»
D£®KÓėĀČĘų·“Ӧɜ³ÉKCl£¬¹ŹD²»Ń”£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģā漲齚ŹōµÄŠŌÖŹ¼°Ńõ»Æ»¹Ō·“Ó¦£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĪļÖŹµÄŠŌÖŹ”¢·¢ÉśµÄ·“Ó¦µČĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāŃõ»Æ»¹Ō·“Ó¦µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
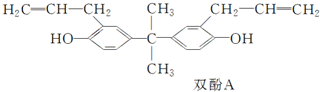
| A£® | Ė«·ÓA·Ö×ÓÖŠĖłÓŠŌ×Ó²»æÉÄÜŌŚŅ»øöĘ½ĆęÉĻ | |
| B£® | Ė«·ÓA·Ö×ÓŹ½ĪŖC21H24O2 | |
| C£® | Ė«·ÓAæÉŅŌ·¢Éś¾ŪŗĻ·“Ó¦ | |
| D£® | 1 molĖ«·ÓA×ī¶ąæÉÓė4 molÅØäåĖ®·¢ÉśČ”“ś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2 | B£® | 16 | C£® | 26 | D£® | 46 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol A Óė×ćĮæµÄĖį·“Ӧɜ³ÉµÄH2±Č1 mol BÉś³ÉµÄH2¶ą | |
| B£® | AŌ×Óµē×Ó²ćŹż±ČBŌ×ӵĵē×Ó²ćŹż¶ą | |
| C£® | ³£ĪĀŹ±£¬AÄÜ“ÓĖ®ÖŠÖĆ»»³öĒā£¬¶ųB²»ÄÜ | |
| D£® | AŌ×ÓµÄ×īĶā²ćµē×ÓŹż±ČBŌ×ÓµÄ×īĶā²ćµē×ÓŹżÉŁ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓÉ·Ēµē½āÖŹČÜÓŚĖ®µĆµ½µÄČÜŅŗ | |
| B£® | ½«pH=9µÄÉÕ¼īČÜŅŗĻ”ŹĶ100±¶ĖłµĆµ½µÄČÜŅŗ | |
| C£® | µČĪļÖŹµÄĮæµÄĒæĖįÓėĒæ¼ī·“Ó¦µĆµ½µÄČÜŅŗ | |
| D£® | c£ØH+£©”¢c£ØOH-£©¾łĪŖ5.0”Į10-7mol•L-1µÄČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
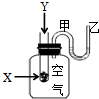 ĪŖĮĖŃŠ¾æ»Æѧ·“Ó¦X+Y=ZµÄÄÜĮæ±ä»ÆĒéæö£¬Ä³Ķ¬Ń§Éč¼ĘĮĖČēĶ¼ĖłŹ¾×°ÖĆ£®µ±ĻņŹ¢ÓŠXµÄŹŌ¹ÜÖŠµĪ¼ÓŹŌ¼ĮYŹ±£¬æ“µ½UŠĶ¹ÜÖŠ¼×“¦ŅŗĆęĻĀ½µŅŅ“¦ŅŗĆęÉĻÉż£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
ĪŖĮĖŃŠ¾æ»Æѧ·“Ó¦X+Y=ZµÄÄÜĮæ±ä»ÆĒéæö£¬Ä³Ķ¬Ń§Éč¼ĘĮĖČēĶ¼ĖłŹ¾×°ÖĆ£®µ±ĻņŹ¢ÓŠXµÄŹŌ¹ÜÖŠµĪ¼ÓŹŌ¼ĮYŹ±£¬æ“µ½UŠĶ¹ÜÖŠ¼×“¦ŅŗĆęĻĀ½µŅŅ“¦ŅŗĆęÉĻÉż£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 9 | B£® | 8 | C£® | 17 | D£® | 25 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
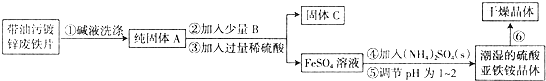
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com