
有4组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如下表所示:
第一组 | He -268.8 | (a) -249.5 | Ar -185.8 | Kr -151.7 |
第二组 | F2 -187.0 | Cl2 -33.6 | (b) 58.7 | I2 184.0 |
第三组 | (c) 19.4 | HCl -84.0 | HBr -67.0 | HI -35.3 |
第四组 | H2O 100.0 | H2S -60.2 | (d) 42.0 | H2Te -1.8 |
下列各项判断正确的是
A.abc的化学式分别为Ne2、Br2、HF
B.第三组与第四组相比较,化合物的稳定顺序为:HBr>d
C.第三组物质溶于水后,溶液的酸性:c>HCl>HBr>HI
D.第四组物质中H2O的沸点最高,是因为H2O分子内存在氢键
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
| 第一组 | He-268.8 | (a)-249.5 | Ar-185.8 | Kr-151.7 |
| 第二组 | F2 -187.0 | Cl2 -33.6 | (b) 58.7 | I2 184.0 |
| 第三组 | (c) 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | (d) 42.0 | H2Te-1.8 |
| A、abc的化学式分别为Ne2、Br2、HF |
| B、第三组与第四组相比较,化合物的稳定顺序为:HBr>d |
| C、第三组物质溶于水后,溶液的酸性:c>HCl>HBr>HI |
| D、第四组物质中H2O的沸点最高,是因为H2O分子内存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为周期表中原子体积(单质原子的摩尔体积)随原子
序数变化的关系。
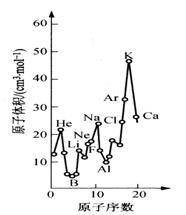 (1)第二周期原子体积最大的元素形成的固态单质属于
(1)第二周期原子体积最大的元素形成的固态单质属于
_________________晶体。第三周期原子体积最小的
元素核外电子排布式为________________________。
(2)试预测下列元素原子体积的关系:Se _____ Br;
Xe _____ Ba(选填 >、 = 或 < )。
(3)从图中可以得出的结论有__________(选填代号)。
a. 同一周期中,原子体积先由大变小,而后又
由小变大
b. 同周期金属元素中,碱金属的原子体积最大
c. 同一主族中从上到下,原子体积一般总是逐
渐减小
(4)由此可见,在元素周期表中,元素性质与它们
所形成的单质和化合物的性质均有周期性变
化规律。试写出一条ⅦA族元素所形成的化
合物某种性质的变化规律:
_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com