
(8分)把1.12 升(标准状况下)HCl气体溶于水,配制成250 mL的溶液,计算:
(1)该溶液中HCl的物质的量浓度。
(2)若将该溶液与足量的锌反应,在标准状况下能生成氢气多少升?
科目:高中化学 来源:2014-2015学年甘肃省高二第一学期期中考试化学试卷(解析版) 题型:选择题
根据碘与氢气反应的热化学方程式(i) I2(g)+H2(g) 2HI(g) △H= - 9.48kJ/mol (ii) I2(s)+H2(g)
2HI(g) △H= - 9.48kJ/mol (ii) I2(s)+H2(g) 2HI(g) △H=+ 26.48kJ/mol。下列判断正确的是
2HI(g) △H=+ 26.48kJ/mol。下列判断正确的是
A.254g I2(g)中通入2g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1mol气态碘所含的能量相差l7.00 kJ
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(i) 拆开1mol I-I键与1mol H-H键需要的总能量小于拆开2mol H-I键需要的总能量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高一上学期期中考试化学试卷(解析版) 题型:填空题
(6分)除去括号内的杂质,写出所加试剂的化学式⑴Cl-(SO42-) : ⑵SO42-(CO32-) : ⑶ Fe2+(Cu2+) :
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高一上学期期中考试化学试卷(解析版) 题型:选择题
将3.22克Na2SO4 ·10H2O 溶于水中,要使Na+离子数目与水分子数目之比为1:100,则加入水的质量为( )克
A.18 B.36 C 34.2 D.37.8
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列各物质,按单质、化合物、混合物的顺序排列的是( )
A.干冰、铁、胆矾 B.液态氧、氧化钙、石灰水
C.氮气、氯化氢、烧碱 D.水、碘酒、熟石灰
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃甘谷县第一中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
300 mL某浓度的NaOH溶液中含有60 g溶质,现欲配制1 mol·L-1NaOH溶液,应取原溶液与蒸馏水的体积比约为
A.1∶4 B.1∶5 C.2∶1 D.2∶3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃甘谷县第一中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.1 mol H2O的质量为18g/mol
B.3.01×1023个SO2分子的质量为32g
C.CH4的摩尔质量为16g
D.标准状况下,1 mol任何物质体积均为22.4L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃天水市高二上第一阶段考试卷化学试卷(解析版) 题型:选择题
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:下列描述正确的是 ( )

A.反应开始到10s,用Z表示的反应速率0.158mol/(L·s)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g)  Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南邵阳县石齐学校高二上第一次月考化学(理)试卷(解析版) 题型:填空题
某温度时,在10 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化下表中数据
t/min | X/mol | Y/mol | Z/mol |
0 | 1.00 | 2.00 | 0.00 |
1 | 0.90 | 1.80 | 0.20 |
3 | 0.75 | 1.50 | 0.50 |
5 | 0.65 | 1.30 | 0.70 |
9 | 0.55 | 1.10 | 0.90 |
10 | 0.55 | 1.10 | 0.90 |
14 | 0.55 | 1.10 | 0.90 |
(1) 体系中发生反应的化学方程式是____________;
(2) 计算该反应在0~3 min时间内产物Z的平均反应速率:________;
(3) 该反应达到平衡时反应物X的转化率α等于________;
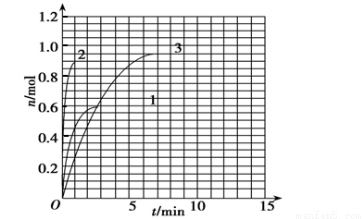
(4) 如果该反应是放热反应,改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1所对应的实验条件改变是:______ ___ ___。
(5)如果起始加入X、Y、Z的物质的量分别为2.00 mol、4.00 mol和0 mol,在原温度下达平衡时,X的转化率为α!,则α! α(填 < > =)。
(6)如果在原温度下起始加入X、Y、Z的物质的量分别为1.00 mol、1.00 mol和1.00 mol,此时可逆反应的反应速率:?(正) ?(逆)(填 < > =)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com