
| A. | 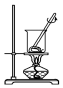 灼烧海带 | B. | 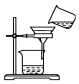 过滤得含I-的溶液 | ||
| C. | 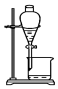 放出碘的苯溶液 | D. | 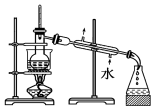 分离碘并回收苯 |
科目:高中化学 来源: 题型:选择题
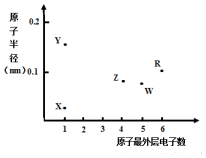 X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示.下列说法错误的是( )
X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示.下列说法错误的是( )| A. | 简单离子半径:Y<W | |
| B. | 最高价氧化物对应水化物的酸性:Z<W | |
| C. | R为氧元素 | |
| D. | X与Z可以形成正四面体结构的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 ml 0.5 mol/L MgCl2 溶液 | B. | 200 ml 0.25 mol/L HCl溶液 | ||
| C. | 50 ml 1 mol/L NaCl溶液 | D. | 200 ml 0.25 mol/L CaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2(g)+Br2(g)?2HBr(g) | B. | 2N2O5(g)=4NO2(g)+O2(g) | ||
| C. | 2SO2(g)+O2?2SO3(g) | D. | CaCO3(s)=CaO(s)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 1:3 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 |
| n(Cl2)/10-3 mol | 0 | 1.8 | 3.7 | 5.4 |
| A. | 0~2 min的反应速率小于4~6 min的反应速率 | |
| B. | 2~6 min用Cl2表示的反应速率为0.9 mol/(L•min) | |
| C. | 降低温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| D. | 平衡常数:K(200℃)<K(400℃) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10gCH4和 10gO2 | B. | 11.2LN2(标准状况)和 11g CO2 | ||
| C. | 9 g H2O 和 0.5mol Cl2 | D. | 224mL H2(标准状况)和 0.1mol N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述实验条件下,物质的氧化性:Cu>SO2>I2 | |
| B. | 在SO2与I2反应中得到的还原产物为H2SO4 | |
| C. | 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 | |
| D. | 滴加KI溶液时.每转移2mole-会生成2molCuI沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com