

| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.8HCl+K2Cr2O7═2KCl+Cr2O3+4H2O+Cl2↑ | ||||
| B.16HCl+2KMnO4═2MnCl2+8H2O+2KCl+5Cl2↑ | ||||
C.4HCl+MnO2
| ||||
| D.6HCl+KClO3═KCl+3H2O+3Cl2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
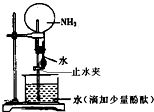
| A.实验正确的操作是先挤压出胶头滴管中的水,再打开止水夹 |
| B.该实验说明氨气是一种极易溶于水的气体,且氨水有碱性 |
| C.将烧瓶中形成的溶液加热,不会发生现象改变 |
| D.形成“喷泉”的原因是氨气溶于水后,烧瓶内的气压小于大气压 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.加热试管中的氯化铵固体制取氨气 |
| B.用锌与稀硝酸反应制取氢气 |
| C.用石灰石与稀盐酸反应制取二氧化碳 |
| D.往过氧化氢中加入少量二氧化锰快速制取少量氧气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
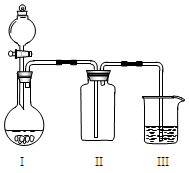
| 选项 | I中的物质 | II中收集的气体 | III中的物质 |
| A | Cu和浓硝酸 | NO | NaOH溶液 |
| B | 浓盐酸和MnO2 | Cl2 | NaOH溶液 |
| C | 碳酸钙和盐酸 | CO2 | 澄清石灰水 |
| D | 浓氨水和CaO | NH3 | 酚酞溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

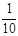 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题: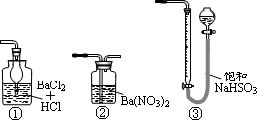
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com