
【题目】在一个固定容积的密闭容器中通入amolN2与bmolH2的混合气体,保持温度不变,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)若反应到某时刻t时,n(N2)=9mol,n(NH3)=2mol,则a=____mol;
(2)反应达平衡时,混合气体的体积为448L(标况下),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量____;
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比、下同),n(始)∶n(平)=____;
(4)原混合气体中,a∶b=_____;
(5)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=_____。
【答案】10 5mol 5:4 2:3 3:3:2
【解析】
(1)根据题意列三段式有:
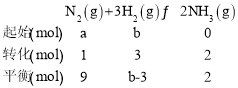
根据三段式可知a=(9+1)mol=10mol;
(2)混合气体的体积为448L(标况下),则混合气体的物质的量为![]() =20mol,NH3的含量(体积分数)为25%,体积分数即物质的量分数,所以n(NH3)=20mol×25%=5mol;
=20mol,NH3的含量(体积分数)为25%,体积分数即物质的量分数,所以n(NH3)=20mol×25%=5mol;
(3)平衡时n(NH3)=5mol,列三段式有

则有(7.5+b-7.5+5)mol=20mol,解得b=15mol,则初始时气体的总物质的量为25mol,所以n(始)∶n(平)=25:20=5:4;
(4)根据2、3小题可知a=10mol,b=15mol,a:b=10:15=2:3;
(5)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=7.5:7.5:5=3:3:2。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】化合物Y是一种常用药物,可由X制得。

下列有关化合物X、Y的说法正确的是
A.由X转化为Y发生取代反应
B.1 mol Y最多可与2 mol NaOH发生反应
C.用银氨溶液可检验X是否完全转化为Y
D.X与足量H2发生反应后,生成的分子中含有6个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素,a、b、c、d的原子序数依次增大。四种元素形成的单质依次为m、n、p、q;x、y、z是这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一;25℃0.01mol·L-1w溶液中,![]() 。上述物质的转化关系如图所示。下列说法正确的是
。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径的大小:a<b<c<d B. 氢化物的沸点:b>d
C. x的电子式为:![]() D. y、w含有的化学键类型完全相同
D. y、w含有的化学键类型完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于甲烷分子结构的说法正确的是( )
A.CH4有还原性,可使酸性高锰酸钾溶液褪色
B.甲烷的电子式为![]() ,分子中各原子都达到“8电子”稳定结构
,分子中各原子都达到“8电子”稳定结构
C.CH3Cl只有一种结构,说明甲烷是以碳原子为中心的正四面体结构
D.做CH4与Cl2发生取代反应实验时,应将反应装置放在光亮的地方
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E原子序数依次增大。A、E同主族,E原子最外层上的电子数是D原子最外层电子数的4倍,D离子与C2-具有相同核外电子排布。
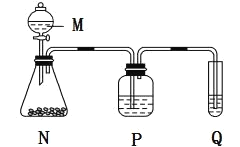
试回答下列问题:
(1)元素E在元素周期表中的位置是______。
(2)A和E最高价氧化物对应的水化物,酸性较弱的为_____。若用图中装置验证这两种酸的酸性强弱,则在仪器P中加入的试剂为_____,Q中观察到的实验现象是_____。
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A、C、D的盐 |
b | C、D组成的化合物,且原子数之比为1∶1 |
c | 化学组成为AC2 |
①a含有的化学键有_____。
②b与c反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl-、CO![]() 、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序中,正确的是( )
、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序中,正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②③②①
C.①②③②④D.④②①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NiOOH难溶于水,常作电池的正极材料。利用某含镍废料(主要成分为NiO,另含有SiO2、Fe2O3、CuO三种杂质)制备NiOOH的工业流程如图。
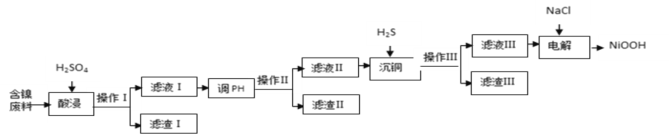
已知:
Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | |
开始沉淀的pH | 1.5 | 4.4 | 6.7 |
沉淀完全的pH | 3.7 | 6.9 | 9.2 |
(1)提高酸浸速度的方法为_______________________、_____________________(任写2条)
(2)滤渣Ⅰ的成分为__________;若滤渣Ⅱ为Fe(OH)3,则“调pH”的范围为_____________.
(3)沉铜时发生反应的离子方程式为______________________________________________。
(4)电解过程是控制在碱性条件下阳极产生ClO-,并用ClO-将Ni2+氧化的过程。请写出氧化过程中发生反应的离子方程式____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】査尔酮类化合物G是黄酮类药物的主要合成中间体,其中一种合成路线如下:
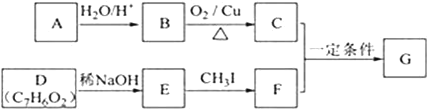
已知以下信息:
①芳香烃A的相对分子质量在100~110之间,1mol A充分燃烧可生成72g水。
②C不能发生银镜反应。
③D能发生银镜反应、可溶于饱和Na2CO3溶液。核磁共振氢谱显示有4种氢。
④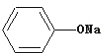 +RCH2I
+RCH2I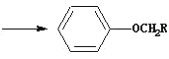
⑤RCOCH3+RˊCHO![]() RCOCH=CHRˊ
RCOCH=CHRˊ
回答下列问题:
(1)A的化学名称为_______。
(2)由B生成C的化学方程式为________。
(3)E的分子式为_______,由E生成F的反应类型为_________。
(4)G的结构简式为______。
(5)D的芳香同分异构体H既能发生银镜反应,又能发生水解反应,H在酸催化下发生水解反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的离子结构示意图为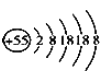 ,该离子显+1价,则该元素在周期表中的位置是( )
,该离子显+1价,则该元素在周期表中的位置是( )
A. 第5周期零族B. 第6周期第IB族
C. 第5周期第ⅦA族D. 第6周期第IA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com