
| A. | 15mol 20% | B. | 20mol 20% | C. | 20mol 80% | D. | 40mol 80% |
分析 固定体积的密闭容器,反应达到平衡时各成分的百分含量与上述平衡时相同,则极限转化为生成物时,生成物的物质的量相同,即起始时充入NH3的物质的量为20mol,
N2+3H2?2NH3
开始 10 30 0
转化 2 6 4
平衡 8 24 4
平衡浓度分别为$\frac{8}{V}$、$\frac{24}{V}$、$\frac{4}{V}$,
K=$\frac{(\frac{4}{V})^{2}}{\frac{8}{V}×(\frac{24}{V})^{3}}$,
2NH3?N2+3H2
开始 20 0 0
转化 2x x 3x
平衡 20-2x x 3x
平衡浓度分别为$\frac{(20-2x)}{V}$、$\frac{x}{V}$、$\frac{3x}{V}$
K1=$\frac{\frac{x}{V}×(\frac{3x}{V})^{3}}{(\frac{20-2x}{V})^{2}}$,
温度不变时,二者互为逆反应,平衡常数K互为倒数关系,以此计算.
解答 解:固定体积的密闭容器,反应达到平衡时各成分的百分含量与上述平衡时相同,则极限转化为生成物时,生成物的物质的量相同,即起始时充入NH3的物质的量为20mol,
N2+3H2?2NH3
开始 10 30 0
转化 2 6 4
平衡 8 24 4
平衡浓度分别为$\frac{8}{V}$、$\frac{24}{V}$、$\frac{4}{V}$,
K=$\frac{(\frac{4}{V})^{2}}{\frac{8}{V}×(\frac{24}{V})^{3}}$,
2NH3?N2+3H2
开始 20 0 0
转化 2x x 3x
平衡 20-2x x 3x
平衡浓度分别为$\frac{(20-2x)}{V}$、$\frac{x}{V}$、$\frac{3x}{V}$
K1=$\frac{\frac{x}{V}×(\frac{3x}{V})^{3}}{(\frac{20-2x}{V})^{2}}$,
温度不变时,二者互为逆反应,平衡常数K互为倒数关系,
则$\frac{(\frac{4}{V})^{2}}{\frac{8}{V}×(\frac{24}{V})^{3}}$×$\frac{\frac{x}{V}×(\frac{3x}{V})^{3}}{(\frac{20-2x}{V})^{2}}$=1,
解得x=8,
达到平衡时NH3的转化率是$\frac{2×8mol}{20mol}$×100%=80%,
故选C.
点评 本题考查化学平衡的计算,为高频考点,把握等效平衡判定、互为逆反应的K的关系为解答的关键,侧重分析与计算能力的考查,注意K的计算,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
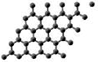
| A. | 石墨烯导电属于化学变化 | B. | 石墨烯与金刚石结构相同 | ||
| C. | 纤维素与淀粉互为同分异构体 | D. | 纤维素属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑥ | B. | ②③④ | C. | ②④⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地壳中金属元素的含量 | B. | 金属的延展性 | ||
| C. | 金属的导电性 | D. | 金属活动性及冶炼的难易程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe (OH )3 溶于稀 H 2 SO4 中:H++OH-→H2O | |
| B. | 氨水滴入 AlCl 3 溶液中:Al3++3OH-→Al(OH)3↓ | |
| C. | FeO 溶于稀 HCl 中:O2-+2H+→H2O | |
| D. | 铝溶解在 NaOH 溶液中:2Al+2OH-+2H2O→2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发展循坏经济,构建资源节约型社会及开发清洁生产技术 | |
| B. | 用绿色化学生产工艺,建立环境友好型化工体系 | |
| C. | 大力开发可再生资源,推广使用乙醇汽油代替传统的燃油 | |
| D. | 设计化学实验方案时,提倡用尽可能多的样品和试剂以提高实验效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 反应达到平衡时,X的转化率为50% | |
| B. | 反应可表示为X+3Y?2Z,平衡常数为1600 | |
| C. | 其他条件不变时,增大压强可使平衡常数增大 | |
| D. | 改变温度可以改变该反应的平衡常数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com