

| A. | 离子半径:W2->Y2+ | |
| B. | 电解X与Z形成的化合物的水溶液,不能得到X单质 | |
| C. | 碘的氢化物酸性比M的氢化物酸性弱 | |
| D. | 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料 |
分析 W、X、Y、Z、N六种主族元素,由元素在周期表的位置可知,X为Na,Y为Mg,W为O,Z为S,M为Cl,N为Ge,然后结合元素周期律来解答.
解答 解:W、X、Y、Z、N六种主族元素,由元素在周期表的位置可知,X为Na,Y为Mg,W为O,Z为S,M为Cl,N为Ge,
A.具有相同电子排布的离子中原子序数大的离子半径小,则离子半径:W2->Y2+,故A正确;
B.X与Z形成的化合物为Na2S,电解其水溶液,生成NaOH、氢气、S,不能得到X单质,故B正确;
C.H-I键长比H-Cl 键长长,则H-I键易断裂,则碘的氢化物酸性比M的氢化物酸性强,故C错误;
D.元素N位于金属与非金属的分界线附近,具有金属性和非金属性,可以推断N元素的单质可作半导体材料,故D正确;
故选C.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素化合物为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 组合序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ |
| 组合数据 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
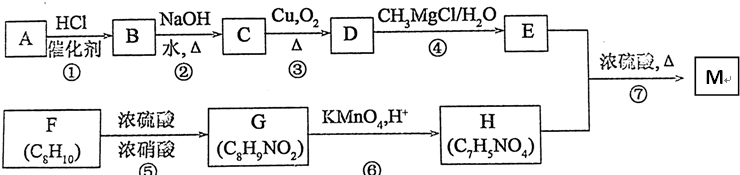
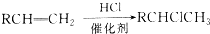
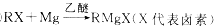
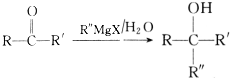
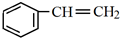 ,C中官能团的名称为羟基.
,C中官能团的名称为羟基.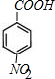 +
+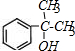 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O. 、
、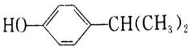 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、Cl2、H2S | B. | O2、H2、SO2 | C. | CH4、HCl、NH3 | D. | NO、SO3、O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
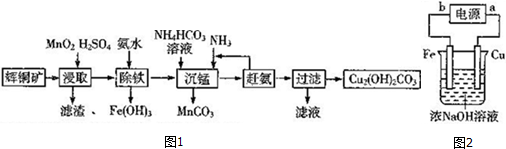
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | [ZnCl4]2-空间构型呈平面四边形 | |
| B. | [ZnCl4]2-空间构型呈正四面体形 | |
| C. | [ZnCl4]2-离子中存在2个σ键和2个π键 | |
| D. | [ZnCl3F]2-不存在着同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 美国一些科学家开发利用人体能,一些超级市场将顾客拉门消耗的能量贮存起来转化为电能,用于超级市场的电能消耗 | |
| B. | 英国农村大面积种植油菜,用植物油代替石油 | |
| C. | 英国科学家对一种嗜热链球菌进行基因移植后,新繁殖后的大量细菌在较高温度下,把稻草中的植物纤维转变为乙醇 | |
| D. | 英美科学家在酶的作用下将水分解成氢气和氧气,利用其释放的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
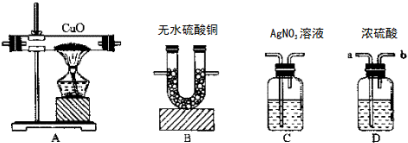
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com