
【题目】下列四组物质中:A.![]() 和
和![]() B.
B. ![]() 和
和![]() C.
C.![]() 和
和![]() D.
D. ![]() 和
和![]() E.
E. ![]() 和
和![]() 。其中__________互为同位素;___________是同分异构体;___________是同系物。
。其中__________互为同位素;___________是同分异构体;___________是同系物。
科目:高中化学 来源: 题型:
【题目】埋在地下的钢管道可以用如图所示方法进行电化学保护,下列说法正确的是( )
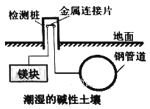
A.钢管道表面发生了还原反应
B.该方法将电能转化为了化学能
C.该方法称为外加电流阴极保护法
D.镁块上发生的电极反应:O2+2H2O+4e→4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题。
(1)含碳量在0.03%2%之间某合金,是目前使用量最大的合金,这种合金是___。
A.铝合金 B.青铜 C.镁合金 D.钢
(2)FeCl3溶液用于腐蚀铜箔印刷线路板,反应的离子方程式为___。
(3)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是__(填字母),大量增加的离子有___(填化学式)。
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(4)4Fe(NO3)2的高纯度结晶体是一种紫色潮解性固体,适合于制磁性氧化铁纳米粉末,工业上用废铁屑(含Fe和Fe2O3及其它不反应的物质)制取Fe(NO3)2晶体的方法如图:
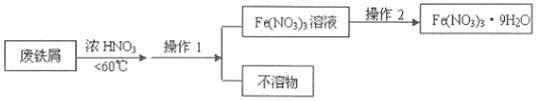
①第1步反应若温度过高,将导致硝酸分解,浓硝酸受热分解的化学方程式为___。
②磁性氧化铁的化学式为___,试写出Fe2O3与硝酸反应的离子方程式___。
③操作1的名称为___,操作2的步骤为:___、___,过滤洗涤。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为解决燃料危机和温室效应,科学家尝试用CO2与CH4制取CO和H2。
(1)已知:①CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1=+206.1kJ·mol-1
CO(g)+3H2(g) ΔH1=+206.1kJ·mol-1
②2H2(g)+CO(g)![]() CH3OH(1) ΔH2=-128.3kJ·mol-1
CH3OH(1) ΔH2=-128.3kJ·mol-1
③2H2(g)+O2(g)![]() 2H2O(g) ΔH3=-483.6kJ·mol-1
2H2O(g) ΔH3=-483.6kJ·mol-1
④2CH4(g)+O2(g)![]() 2CH3OH(1) △H4
2CH3OH(1) △H4
在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇在低温下能否自发进行____(填“能”或“否”),理由是____。
(2)某温度下,CH4(g)+H2O(g)![]() CO(g)+3H2(g),将1molCH4(g)和1molH2O(g)加入100kPa的密闭容器中,正反应速率v正=k正×p(CH4)×p(H2O),逆反应速率v逆=k逆×p(CO)×p3(H2),p为分压(分压=总压×物质的量分数),则该反应的压强平衡常数Kp=____(以k正、k逆表示)。若k正=4.4×104kPa-1·s-1,当CH4分解20%时,v正=____kPa·s-1(保留两位有效数字)。
CO(g)+3H2(g),将1molCH4(g)和1molH2O(g)加入100kPa的密闭容器中,正反应速率v正=k正×p(CH4)×p(H2O),逆反应速率v逆=k逆×p(CO)×p3(H2),p为分压(分压=总压×物质的量分数),则该反应的压强平衡常数Kp=____(以k正、k逆表示)。若k正=4.4×104kPa-1·s-1,当CH4分解20%时,v正=____kPa·s-1(保留两位有效数字)。
(3)CO2用于生产乙烯,已知:2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ΔH=QkJ/mol。
CH2=CH2(g)+4H2O(g) ΔH=QkJ/mol。
一定条件下,按不同的投料比![]() 向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。

①X1____X2(填“>”或“<”,后同),Q____0。
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为_____。
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-)∶c(HCO3-)=____。
[常温下K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11]。
②欲用5LNa2CO3溶液将23.3gBaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为____。[已知:常温下Ksp(BaSO4)=1×10-7、Ksp(BaCO3)=2.5×10-6]。(忽略溶液体积的变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳氢化合物又称为烃,烃分为饱和烃和不饱和烃两大类。完成下列填空:
(1)能与乙烯发生加成反应的物质是_______(填写编号)。
a. 溴水 b. 氧气 c. 氯化氢 d. 酸性高锰酸钾溶液
(2)与乙烯和氢气的加成产物互为同系物的是________(填写编号)。
a. ![]() b.
b. ![]() c.
c. ![]() d.
d. ![]()
(3)请写出乙烯相邻同系物的加聚反应方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图
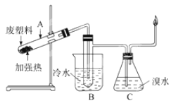
加热聚丙烯废塑料得到的产物如表:
产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔:
![]()
写出反应(2)的化学方程式__________________________________。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有____种。
(3)经锥形瓶C中溴水充分吸收,剩余气体经过干燥后的平均相对分子质量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示:

关于咖啡鞣酸的下列叙述正确的是( )
A.分子式为C16H13O9
B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应
C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键
D.与浓溴水能发生两种类型的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr![]() C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?_____________。
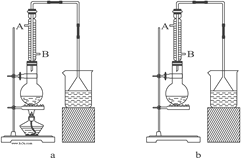
(2)反应装置中的烧瓶应选择下列哪种规格最合适(_____)
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是(_____)
A. A进B出 B. B进A出 C. 从A进或B进均可
(4)可能发生的副反应为:_____________、__________、______________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于一些重要的化学概念有下列说法,其中正确的是( )
①Fe(OH)3胶体和CuSO4溶液都是混合物 ②BaSO4是一种难溶于水的强电解质 ③冰醋酸、纯碱、小苏打分别属于酸、碱、盐 ④煤的干馏、煤的气化和液化都属于化学变化 ⑤置换反应都属于离子反应
A.①②⑤B.①②④C.②③④D.③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com