
【题目】乙二酸二乙酯(D)可由石油气裂解得到的烯烃合成.回答下列问题:

(1)B和A为同系物,B的结构简式为 .
(2)反应①的化学方程式为 ,其反应类型为 .
(3)反应③的反应类型为 .
(4)C的结构简式为 .
(5)反应②的化学方程式为 .
【答案】(1)CH2=CHCH3;
(2)CH2=CH2+H2O![]() CH3CH2OH,加成反应;
CH3CH2OH,加成反应;
(3)水解反应或取代反应;
(4)HOOC﹣COOH;
(5)HOOC﹣COOH+2CH3CH2OH![]() CH3CH2OOCCOOCH2CH3+2H2O.
CH3CH2OOCCOOCH2CH3+2H2O.
【解析】
试题分析:C2H6O与C反应生成D,由D的结构简式可知C为HOOC﹣COOH,C2H6O为CH3CH2OH,则A为CH2=CH2,与水发生加成反应生成乙醇.C3H5Cl发生卤代烃的水解反应生成CH2=CHCH2OH,则C3H5Cl为CH2=CHCH2Cl,B为CH2=CHCH3,CH2=CHCHO发生氧化反应得到HOOC﹣COOH.
解:C2H6O与C反应生成D,由D的结构简式可知C为HOOC﹣COOH,C2H6O为CH3CH2OH,则A为CH2=CH2,与水发生加成反应生成乙醇.C3H5Cl发生卤代烃的水解反应生成CH2=CHCH2OH,则C3H5Cl为CH2=CHCH2Cl,B为CH2=CHCH3,CH2=CHCHO发生氧化反应得到HOOC﹣COOH.
(1)由上述分析可知,B的结构简式为:CH2=CHCH3,
故答案为:CH2=CHCH3;
(2)反应①是CH2=CH2和水发生加成反应生成乙醇,化学方程式为:CH2=CH2+H2O![]() CH3CH2OH,属于加成反应,
CH3CH2OH,属于加成反应,
故答案为:CH2=CH2+H2O![]() CH3CH2OH,加成反应;
CH3CH2OH,加成反应;
(3)反应③是CH2=CHCH2Cl发生水解反应生成CH2=CHCH2OH,也属于取代反应,
故答案为:水解反应或取代反应;
(4)C的结构简式为:HOOC﹣COOH,
故答案为:HOOC﹣COOH;
(5)反应②是乙二酸与乙醇发生酯化反应生成乙二酸二乙酯,化学方程式为:HOOC﹣COOH+2CH3CH2OH![]() CH3CH2OOCCOOCH2CH3+2H2O,
CH3CH2OOCCOOCH2CH3+2H2O,
故答案为:HOOC﹣COOH+2CH3CH2OH![]() CH3CH2OOCCOOCH2CH3+2H2O.
CH3CH2OOCCOOCH2CH3+2H2O.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氮的化合物合成、应用及氮的固定一直是科学研究的热点。
(1)以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);ΔH=a kJ·mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98 kJ·mol-1
则a为 。
(2)反应2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(g)在合成塔中进行。下图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比 [n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
CO(NH2)2(l)+H2O(g)在合成塔中进行。下图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比 [n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
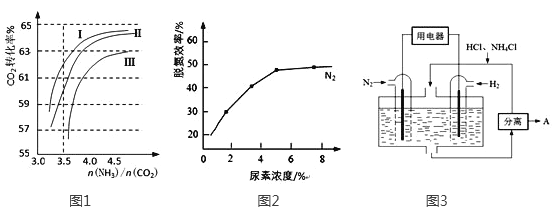
①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值分别为:
A. 0.6~0.7 B. 1~1.1 C. 1.5~1.61
生产中应选用水碳比的数值为 (选填序号)。
②生产中氨碳比宜控制在4.0左右,而不是4.5的原因可能是 。
(3)尿素可用于湿法烟气脱氮工艺,其反应原理为:
NO+NO2+H2O=2HNO22HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
①当烟气中NO、NO2按上述反应中系数比时脱氮效果最佳。若烟气中V(NO)∶V(NO2)=5∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)= (空气中氧气的体积含量大约为20%)。
②图2是尿素含量对脱氮效率的影响,从经济因素上考虑,一般选择尿素浓度约为 %。
(4)图3表示使用新型电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池。请写出该电池的正极反应式 。生产中可分离出的物质A的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关右图装置的叙述中,正确的是( )
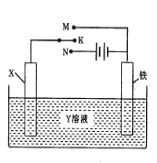
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为外接电源的阴极保护法
B.若X为碳棒,Y为饱和NaOH溶液,开关K置于N处,保持温度不变,则溶液的pH保持不变
C.若X为银棒,Y为硝酸银溶液,开关K置于N处,铁棒质量将增加,溶液中银离子浓度将减小
D.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铁电极移动[来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应中的能量变化,表述正确的是( )
A.放热反应中,反应物的总能量大于生成物的总能量
B.断开化学键的过程会放出能量
C.加热才能发生的反应一定是吸热反应
D.氧化反应均为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几组物质,请将序号填入下列空格内:
A、CH2=CH﹣COOH和油酸(C17H33COOH)
B、12C60和石墨
C、![]() 和
和![]()
D、35Cl和37Cl
E、乙醇和乙二醇
(1)互为同位素的是 ;
(2)互为同系物的是 ;
(3)互为同素异形体的是 ;
(4)互为同分异构体的是 ;
(5)既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列几个装置示意图,有关叙述正确的是 ( )

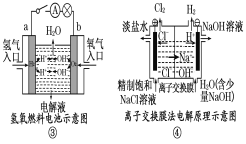
A.装置①中阳极上析出红色固体
B.装置②的待镀铁制品应与电源负极相连
C.装置③中外电路电子由a极流向b极
D.装置④的阳极反应为:2H+ + 2e— = H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加快的是( )
A.加热 B.不用稀硫酸,改用98%浓硫酸
C.滴加少量CuSO4溶液 D.不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按原子序数递增,下列有关碱金属元素性质的递变规律正确的是( )
A. 失电子能力逐渐增强
B. 化合价逐渐升高
C. 金属性逐渐减弱
D. 最高价氧化物对应的水化物碱性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4是一种典型的强氧化剂。请回答下列问题:
(1)实验室中可用已知浓度的酸性高锰酸钾溶液滴定含Fe2+的溶液,从而测定溶液中Fe2+的浓度,离子反应方程式如下,请在空格内填上缺少的反应物,并配平:
_______-Fe2++_______MnO![]() +_______
+_______![]() ===_______Fe3++_______Mn2++_______H2O
===_______Fe3++_______Mn2++_______H2O
(2)在稀硫酸中,MnO![]() 和H2O2也能发生氧化还原反应:
和H2O2也能发生氧化还原反应:
氧化反应:H2O2-2e-===2H++O2↑
还原反应:MnO![]() +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
①写出该氧化还原反应的化学方程式:__________________。
反应中若有0.5 mol H2O2参加此反应,转移电子的个数为________。
②实验中发现,当加入的少量KMnO4完全反应后,H2O2仍能发生反应快速放出气体。其可能的原因是__________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com