



 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
| A、1 L 1mol?L-1CaCl2溶液中含有的氯离子数为2NA |
| B、锌从盐酸中置换出1 mol H2,电子转移数为NA |
| C、常温常压下,11.2 L氧气含有的原子数为NA |
| D、4.4 g二氧化碳含有的原子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加硫酸的序号 | 加入硫酸的体积m/L | 剩余固体的质量/g |
| 1 | 20.0 | 7.20 |
| 2 | 20.0 | 4.40 |
| 3 | 20.0 | 2.00 |
| 4 | 20.0 | 2.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
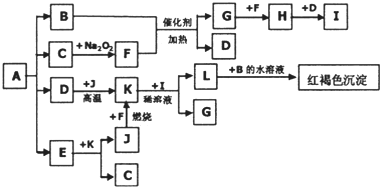
查看答案和解析>>
科目:高中化学 来源: 题型:
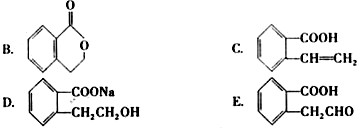
查看答案和解析>>
科目:高中化学 来源: 题型:
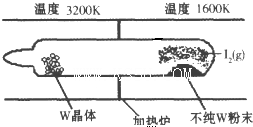 化学反应原理在科研和生产中有广泛应用.
化学反应原理在科研和生产中有广泛应用.| 1 |
| 2 |
c(S
| ||
c(HS
|
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH(25℃) | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com