
【题目】化合物H是合成治疗心血管疾病药物的中间体,可通过以下途径合成:

已知:① (苯胺易被氧化)
(苯胺易被氧化)
②甲苯发生一硝基取代反应与A类似。
回答下列问题:
(1)写出C中官能团的名称:___________。
(2)写出有关反应类型:B![]() C _______;F
C _______;F![]() G______ o
G______ o
(3)写出A![]() B的反应方程式:___________ 。
B的反应方程式:___________ 。
(4)写出同时满足下列条件D的所有同分异构体的结构简式:_______________
①能发生银镜反应
②能发生水解反应,水解产物之一与FeCl3溶液反应显紫色
③核磁共振氢谱(1![]() 显示分子中有4种不同化学环境的氢
显示分子中有4种不同化学环境的氢
(5)合成途径中,C转化为D的目的是___________________
(6)参照上述合成路线,以甲苯和![]() 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备 的合成路线。__________
的合成路线。__________
【答案】氨基、醚键 还原反应 消去反应 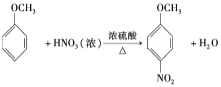
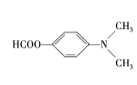 、
、 、
、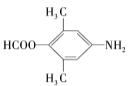 保护氨基,防止合成过程中被氧化
保护氨基,防止合成过程中被氧化 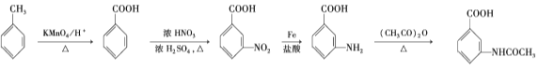
【解析】
根据合成路线中各中间产物的结构特点及反应条件分析每步合成的产物及反应类型;根据官能团的性质按照已知条件书写同分异构体;运用逆合成分析法,结合题干信息设计合成路线。
根据A、C的结构简式及题干信息知B为![]() ,B→C的过程是硝基转化为氨基,属于还原反应,比较C和D的结构变化知,该反应为取代反应,比较E和G的结构简式得F的结构简式为
,B→C的过程是硝基转化为氨基,属于还原反应,比较C和D的结构变化知,该反应为取代反应,比较E和G的结构简式得F的结构简式为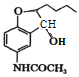 ,F→G为消去反应,G到H为水解反应;
,F→G为消去反应,G到H为水解反应;
(1)根据C的结构简式知官能团的名称为氨基、醚键;
(2)B→C的过程是硝基转化为氨基,属于还原反应;F→G脱水形成双键,为消去反应;
(3)A![]() B为硝化反应,方程式为:
B为硝化反应,方程式为: ;
;
(4)①能发生银镜反应,则结构中含有醛基;②能发生水解反应,水解产物之一与FeCl3溶液反应显紫色,则结构中含由酚羟基形成的酯基;③核磁共振氢谱有4种不同化学环境的氢,说明结构具有一定对称性,则该结构可能为: 、
、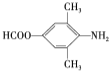 、
、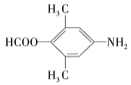 ;
;
(5)根据合成途径中的最终产物结构及题干信息分析知,C转化为D的目的是保护氨基,防止合成过程中被氧化;
(6)参照上述合成路线结合已知①②,用逆合成分析法知目标产物可以由间氨基苯甲酸与(CH3CO)2O发生取代反应得到,而间氨基苯甲酸可以通过间硝基苯甲酸还原得到,间硝基苯甲酸由苯甲酸硝化反应得到,苯甲酸可以由甲苯氧化得到,设计合成路线为:
 。
。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O![]() Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2 -e— + OH- = NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化锶(Sr3N2)在工业上广泛用于生产荧光粉。已知:锶与镁位于同主族:锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应。

I.利用装置A和C制备Sr3N2
(1)实验装置中玻璃管之间需用橡皮管连接,其连接方法是先将___________,然后稍稍用力即可将玻璃管插入橡皮管。
(2)写出由装置A制备N2的化学反应方程式___________。
(3)装置A中a导管的作用是________。利用该套装置时,有同学提出应先点燃置A的酒精灯一段时间后,再点燃装置C的酒精灯,你同意其观点吗?_______(“同意”或“不同意”)。理由是___________。
Ⅱ.利用装置B和C制备Sr3N2。利用装置B从空气中提纯N2(已知:氧气可被连苯三酚溶液定量吸收)
(4)写出装置B的NaOH溶液中发生反应的离子方程式___________。
(5)装置C中广口瓶盛放的试剂是___________。
Ⅲ.测定Sr3N2产品的纯度
(6)取10.0g该产品,向其中加入适量的水,将生成的气体全部通入浓硫酸中,利用浓硫酸增重质量计算得到产品的纯度,该方法测得产品的纯度偏高,其原因是_______。经改进后测得浓硫酸增重1.02g,则产品的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是某学生设计的实验室制备并干燥Cl2及吸收多余氯气的实验装置图,请回答:

(1)指出上图中的各处错误:
①____________________________________________________
②____________________________________________________
③____________________________________________________
④____________________________________________________
(2)制备实验开始时,先检查装置的气密性,接下来的操作依次是 ________
A、向烧瓶中加入MnO2粉末 B、加热 C、向烧瓶中加入浓盐酸
(3)如果将过量二氧化锰与20mL 12mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol。其主要原因有:
①____________________________________________________
②____________________________________________________
(4)为了提高浓盐酸的利用率,你对实验的建议是:
①____________________________________________________
②____________________________________________________
(5)写出圆底烧瓶中发生反应的离子反应方程式,并用单线桥表示电子转移的方向和数目________________
(6)NaClO是84消毒液的有效成分。请回答下列问题
①浸泡衣物时加入84消毒液在空气中放置一段时间漂白效果更好,结合离子方程式解释原因 ____________(已知酸性:H2CO3 >HClO>HCO3-)
②若将84消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是____________________________________________;
(7)Cl2是一种有毒气体,如果泄露会造成严重的危害。
①已知:3Cl2 + 8NH3 = 6NH4Cl +N2,化工厂可用浓氨水来检验Cl2是否泄露,该反应中被氧化和未被氧化的NH3的物质的量比________ ;
②喷射石灰乳等碱性物质可以减轻少量Cl2泄露造成的危害,Cl2与石灰乳反应的化学方程式是____________
③实验室常用烧碱溶液吸收Cl2,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合溶液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:

已知:①菱锰矿石主要成分是![]() ,还含有少量Fe、Al、Ca、Mg等元素;
,还含有少量Fe、Al、Ca、Mg等元素;
②相关金属离子![]() 形成氯氧化物沉淀时的pH如下:
形成氯氧化物沉淀时的pH如下:
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
③常温下, ![]() 的溶度积分别为
的溶度积分别为![]()
回答下列问题:
(1)“焙烧”时发生的主要化学反应方程式为_____________________。
(2)分析下列图1、图2、图3,氯化铵焙烧菱镁矿的最佳条件是:

焙烧温度_________,氯化铵与菱镁矿粉的质量之比为__________,焙烧时间为___________.
(3)浸出液“净化除杂”过程如下:首先加入![]() 氧化为
氧化为![]() ,反应的离子方程式为________;然后调节溶液pH使
,反应的离子方程式为________;然后调节溶液pH使![]() 沉淀完全,此时溶液的pH范围为____。再加入
沉淀完全,此时溶液的pH范围为____。再加入![]() 沉淀
沉淀![]() ,当
,当![]() 时,
时, ![]() =______
=______![]()
(4)碳化结晶时,发生反应的离子方程式为___________。
(5)流程中能循环利用的固态物质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 表示阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,22.4L CCl4 含有的原子数为 5NA
B.1.8g 的 NH4+中含有的电子数为 NA
C.常温常压下,32 g O2 和 O3 的混合气体中所含原子数为 1.5 NA
D.7.1g Cl2 溶于水,转移电子数目为 0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A为一氯代物,H是通过缩聚反应获得的高聚物。

已知:![]() (苯胺,易被氧化)
(苯胺,易被氧化)
(1)X的结构简式为 。
(2)A的结构简式为 。
(3) G的结构简式为 。反应②③两步能否互换 ,(填“能”或“不能”)理由是 。
(4)反应④的化学方程式是 ;反应⑤的化学方程式是 。
(5)写出同时满足下列条件的阿司匹林的一种同分异构体的结构简式 。
①苯环上一卤代物只有2种;
②能发生银镜反应,分子中无甲基;
③1mol该物质最多能与3molNaOH反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法一定正确的是( )
A. 第ⅠA族碱金属元素与ⅦA族元素所形成的化合物在固态时为离子晶体,晶体中阴、阳离子排列方式相同
B. 晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子
C. 离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键
D. C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有12个

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是碳酸钙(CaCO3)在25 ℃和100 ℃两种情况下,在水中的溶解平衡曲线。下列有关说法正确的是

A. CaCO3(s)![]() Ca2+(aq)+ CO32-(aq) ΔH<0
Ca2+(aq)+ CO32-(aq) ΔH<0
B. a、b、c、d四点对应的溶度积Ksp相等
C. 温度不变,蒸发水,可使溶液由a点变到c点
D. 25 ℃时,CaCO3的Ksp=2.8×10-9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com