
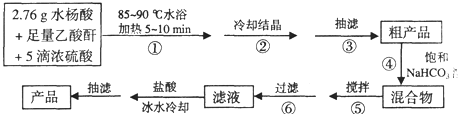
(16分)以下是合成乙酰水杨酸(阿司匹林)的实验流程图,请你回答有关问题:
已知:阿司匹林、水杨酸和乙酸酐的相对分子量分别为:180、138、102。
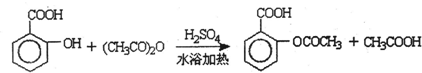
(1)制取阿司匹林的化学反应方程式为_________________;反应类型____________;
(2)水杨酸分子之间会发生缩合反应生成聚合物,写出除去聚合物并提纯阿司匹林的有关离子反应方程式______________________________、____________________________;
(3)阿司匹林在碱性条件下会发生水解反应,请写出阿司匹林与足量NaOH溶液反应的离子方程式______________________________________________________;
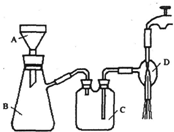
(4)在过程③的抽滤中,用冷水洗涤晶体,其作用_______________________;
(5)根据阿司匹林的结构推测其性质___________;
| A.与纯碱溶液能反应 | B.不能发生加成反应 |
| C.能与氯化铁发生显色反应 | D.水解反应 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:浙江省瑞安中学2011-2012学年高二下学期期末考试化学试题 题型:058
以下是合成乙酰水杨酸(阿司匹林)的实验流程图,请你回答有关问题:

已知:阿司匹林、水杨酸和乙酸酐的相对分子量分别为:180、138、102.
(1)制取阿司匹林的化学反应方程式为________;反应类型________;
(2)水杨酸分子之间会发生缩合反应生成聚合物,写出除去聚合物并提纯阿司匹林的有关离子反应方程式________、________;
(3)阿司匹林在碱性条件下会发生水解反应,请写出阿司匹林与足量NaOH溶液反应的离子方程式________;
(4)在过程③的抽滤中,用冷水洗涤晶体,其作用________;
(5)根据阿司匹林的结构推测其性质________;
A.与纯碱溶液能反应
B.不能发生加成反应
C.能与氯化铁发生显色反应
D.水解反应
E.不能发生银镜反应
F.能发生消去反应
(6)取2.000 g水杨酸、5.400 g乙酸酐反应,最终得到产品1.566 g.求实际产率________;
查看答案和解析>>
科目:高中化学 来源: 题型:
用阿司匹灵治疗头痛、防治心脏病和中风已有百年历史。伦敦帝国学院和哈默史密斯医院前列腺生物学小组的医生们进行的最新研究显示,阿司匹灵还可能阻止或减缓与癌肿瘤增大有关的cox-2酶的生成。阿司匹灵(化学名为:乙酰水杨酸)的结构简式为:![]() 若将阿司匹灵溶于过量的氢氧化钠溶液,其反应的化学方程式为:_________________________
若将阿司匹灵溶于过量的氢氧化钠溶液,其反应的化学方程式为:_________________________
科学家把药物连在高分子载体上,可制成缓释长效药剂。如:阿司匹灵可连接在某高分子聚合物上,形成缓释长效药剂。其中一种的结构简式为:
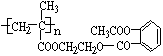
该药体在人体内可能通过水解作用缓缓释放出阿司匹灵,有关的化学方程式:
___________________________________________________
现欲以丙烯为基本原料,通过以下途径合成缓释长效阿司匹灵中的高分子载体。
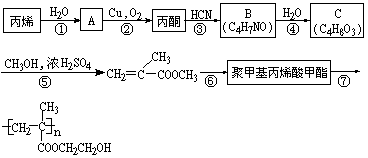
在上述反应中,属于加成反应的有:____________;属于氧化反应的有:____________。
已知:在硫酸存在及加热、加压的条件下,有利于反应①进行。试指出硫酸在该反应过程中所起的作用是什么?____________。加热、加压有利于该反应进行的原因是什么?
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期期末考试化学试卷(解析版) 题型:实验题
(16分)以下是合成乙酰水杨酸(阿司匹林)的实验流程图,请你回答有关问题:
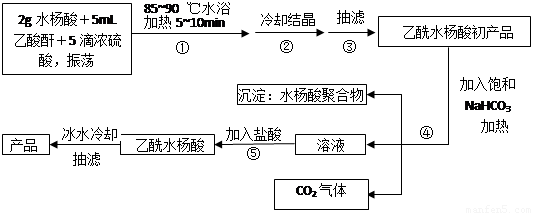
已知:阿司匹林、水杨酸和乙酸酐的相对分子量分别为:180、138、102。
(1)制取阿司匹林的化学反应方程式为_________________;反应类型____________;
(2)水杨酸分子之间会发生缩合反应生成聚合物,写出除去聚合物并提纯阿司匹林的有关离子反应方程式______________________________、____________________________;
(3)阿司匹林在碱性条件下会发生水解反应,请写出阿司匹林与足量NaOH溶液反应的离子方程式______________________________________________________;
(4)在过程③的抽滤中,用冷水洗涤晶体,其作用_______________________;
(5)根据阿司匹林的结构推测其性质___________;
A.与纯碱溶液能反应 B.不能发生加成反应 C.能与氯化铁发生显色反应
D.水解反应 E.不能发生银镜反应 F.能发生消去反应
(6)取2.000 g水杨酸、5.400 g乙酸酐反应,最终得到产品1.566 g。求实际产率_________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com