

试完成下列问题:?
(1)若上述的悬浊液是NaHCO3和NH4Cl的混合物,则I和Ⅱ的总反应式是________________。
(2)由这一反应可知NaCl比NaHCO3溶解度________________。?
(3)操作I、Ⅱ不能颠倒的原因是 ________________。?
(4)Ⅲ的操作叫 ________________;Ⅳ的操作叫 ________________________。?
科目:高中化学 来源: 题型:
 工业上用侯氏制碱法可制得碳酸氢钠晶体,该反应原理可以用以下化学方程式表示:
工业上用侯氏制碱法可制得碳酸氢钠晶体,该反应原理可以用以下化学方程式表示: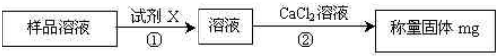
| 21m |
| 25w |
| 21m |
| 25w |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | CO2 | NH3 | NaHCO3 | NH4Cl | NaCl |
| 溶解度(20℃) | V水:V二氧化碳=1:1 | V水:V氯气=1:700 | 9.6g | 37.2g | ag |
查看答案和解析>>
科目:高中化学 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
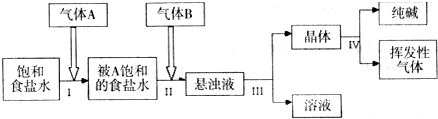
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业作出了突出贡献.他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、氨气为原料先制得NaHCO3,进而生产出纯碱.侯氏制碱法的步骤如下(已知常温下1体积水可溶解700体积NH3).

试完成下列问题:
(1)上述悬浊液是NaHCO3和NH4Cl的混合液,则a和b两步的总反应方程式为:________.
(2)由这一反应可知NaHCO3溶解度比NaCl________.
(3)操作a、b的试剂不能颠倒的原因是________.
(4)操作c称作________,操作d称作________.
查看答案和解析>>
科目:高中化学 来源:四川省广元中学2010届高三第四次月考、化学试卷 题型:058
我国著名化学家侯德榜先生发明的“侯氏制碱法”,因原料利用率高,并能进行连续生产,从而享誉中内外.“侯氏制碱法”的基本做法是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,再将所得碳酸氢钠晶体加热分解后即可得到纯碱.它的反应原理可用下列化学方程式表示:
NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl
2NaHCO3Na2![]() CO3+CO2+H2O
CO3+CO2+H2O
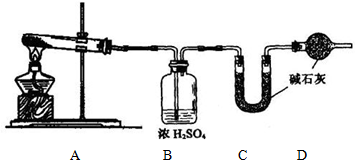
某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如下一套实验装置

实验室可选药品有浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化铵、氯化钠
(1)选用最合适的试剂的名称D________
(2)本实验具体操作过程中,应先通________气体,再通________气体;
(3)指出该装置的三处错误________ ________ ________
(4)在改进装置后,该同学进行了实验,实验所用的饱和NaCl溶液中含溶质58.5 g,实验最后得到无水碳酸钠26 g,则其产率为________;该同学针对其实验结果,认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是________
(5)在“侯氏制碱法”的工业生产中,原料的利用率高,大大降低了成本.请问本实验中哪些物质可重复利用?________
查看答案和解析>>
科目:高中化学 来源: 题型:

试完成下列问题:
(1)上述悬浊液是NaHCO3和NH4Cl的混合液,则a和b两步的总反应方程式为:____________________________________________________________________。
(2)由这一反应可知NaHCO3溶解度比NaCl_______________。
(3)操作a、b的试剂不能颠倒的原因是__________________________________________。
(4)操作c称作_______________,操作d称作_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com