
| A£® | »Æѧ¼ü“ęŌŚÓŚŌ×ÓÖ®¼ä£¬Ņ²“ęŌŚÓŚ·Ö×ÓÖ®¼ä | |
| B£® | Ąė×Ó¼üŹĒŅõ”¢ŃōĄė×ÓÖ®¼äµÄĪüŅżĮ¦ | |
| C£® | Ąė×Ó»ÆŗĻĪļæÉŅŌŗ¬¹²¼Ū¼ü | |
| D£® | ·Ö×Ó¼ä×÷ÓĆĮ¦Ō½“󣬷Ö×ÓŌ½ĪČ¶Ø |
·ÖĪö A”¢»Æѧ¼ü“ęŌŚÓŚ·Ö×ÓÄŚ£¬“ęŌŚÓŚĻąĮŚŌ×ÓÖ®¼ä£»
B”¢ŅõŃōĄė×ÓÖ®¼äµÄĻą»„×÷ÓĆŹĒĄė×Ó¼ü£»
C”¢ĒāŃõ»Æ¼ŲÖŠŗ¬ÓŠĄė×Ó¼üŗĶ¹²¼Ū¼ü£»
D”¢·Ö×ÓµÄĪČ¶ØŠŌŹĒ»ÆѧŠŌÖŹ£»
½ā“š ½ā£ŗA”¢»Æѧ¼ü“ęŌŚÓŚ·Ö×ÓÄŚ£¬“ęŌŚÓŚĻąĮŚŌ×ÓÖ®¼ä£¬²»“ęŌŚ·Ö×Ӽ䣬¹ŹA“ķĪó£»
B”¢ŅõŃōĄė×ÓÖ®¼äµÄĻą»„×÷ÓĆŹĒĄė×Ó¼ü£¬ÕāÖÖĻą»„×÷ÓĆ¼Č°üĄØĪüŅżĮ¦Ņ²°üĄØÅųāĮ¦£¬¹ŹB“ķĪó£»
C”¢Ąė×Ó»ÆŗĻĪļÖŠæÉÄÜŗ¬ÓŠ¹²¼Ū¼ü£¬ČēKOH£¬¹ŹCÕżČ·£»
D”¢·Ö×ÓµÄĪČ¶ØŠŌŹĒ»ÆѧŠŌÖŹ£¬¶ų·Ö×Ó¼ä×÷ÓĆĮ¦ŹĒ¾ö¶ØĪļĄķŠŌÖŹ£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ¼üŗĶ»ÆŗĻĪļµÄ¹ŲĻµ£¬øł¾ŻĪļÖŹÖŠ“ęŌŚµÄ»Æѧ¼ü½įŗĻĄė×Ó»ÆŗĻĪļ”¢¹²¼Ū»ÆŗĻĪļµÄ»ł±¾øÅÄīĄ“·ÖĪö½ā“š£¬×¢Ņā²»ÄÜøł¾ŻŹĒ·ńŗ¬ÓŠ½šŹōŌŖĖŲÅŠ¶ĻĄė×Ó¼ü£¬ĪŖŅדķµć£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 ²»Ņ×±»Ńõ»Æ³ÉōČĖį
²»Ņ×±»Ńõ»Æ³ÉōČĖį ²»Ņ×±»Ńõ»Æ³ÉČ©»ņĶŖ
²»Ņ×±»Ńõ»Æ³ÉČ©»ņĶŖ
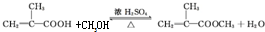 £®
£®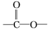 ”±½į¹¹µÄ¹²ÓŠ6ÖÖ£®
”±½į¹¹µÄ¹²ÓŠ6ÖÖ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓƱłĖ®»ģŗĻĪļĄäČ“SO3ĘųĢ壻¼ÓČČI2 | |
| B£® | ľĢæĪüø½NO2ĘųĢ壻½«Cl2ĶØČėĘ·ŗģČÜŅŗÖŠ | |
| C£® | “ņæŖŹ¢ÓŠNOµÄ¼ÆĘųĘ棻ĄäČ“NO2ĘųĢå | |
| D£® | ĻņĘ·ŗģČÜŅŗÖŠĶØČėSO2£¬ĻņFeCl3ČÜŅŗµĪ¼ÓKSCNČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
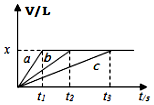 ½«µČĪļÖŹµÄĮæÄĘ”¢Ć¾”¢ĀĮČżÖÖ½šŹō·Ö±šÓė200mL1mol•L-1µÄŃĪĖį·“Ó¦£¬²āµĆÉś³ÉµÄĘųĢåµÄĢå»żV£ØŅŃÕŪŗĻ³É±ź×¼×“æöµÄĢå»ż£©ÓėŹ±¼ätµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
½«µČĪļÖŹµÄĮæÄĘ”¢Ć¾”¢ĀĮČżÖÖ½šŹō·Ö±šÓė200mL1mol•L-1µÄŃĪĖį·“Ó¦£¬²āµĆÉś³ÉµÄĘųĢåµÄĢå»żV£ØŅŃÕŪŗĻ³É±ź×¼×“æöµÄĢå»ż£©ÓėŹ±¼ätµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | x=44.8 | B£® | ·“Ó¦ŗóµÄĆ¾ŗĶĀĮ¾łÓŠŹ£Óą | ||
| C£® | ½šŹōµÄĪļÖŹµÄĮææÉÄܾłĪŖ0.1mol | D£® | ĒśĻßc±ķŹ¾ÄĘÓėŃĪĖįµÄ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ³£ĪĀ³£Ń¹ĻĀ£¬2.8 g N2ŗĶCOµÄ»ģŗĻĘųĢåĖłŗ¬Ō×ÓŹżĪŖ0.2 NA | |
| B£® | 1 mol Cl2Óė×ćĮæFeĶźČ«·“Ó¦£¬×ŖŅĘ3NAøöµē×Ó | |
| C£® | 1 L 0.1 mol•L-1NaHCO3ČÜŅŗÖŠŗ¬ÓŠ0.1 NAøöHCO3- | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬22.4LŅŅĻ©ÖŠC-H¼üŹżĪŖ4NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįÄĘČÜŅŗ³Ź¼īŠŌ£¬æÉÓĆČȵēæ¼īČÜŅŗ³żČ„æóĪļÓĶĪŪ | |
| B£® | Ńõ»ÆĀĮµÄČŪµćŗÜøߣ¬æÉÓĆÓŚÖĘ×÷ÄĶøßĪĀ²ÄĮĻ | |
| C£® | C12”¢SO2¾łÓŠĘư׊Ō£¬æÉŹ¹×ĻÉ«ŹÆČļČÜŅŗĶŹÉ« | |
| D£® | ÄĘµÄ½šŹōŠŌĒæÓŚ¼Ų£¬¹¤ŅµÉĻæÉÓĆÄĘÖĘČ”¼ŲNa+KCl$\frac{\underline{\;850”ę\;}}{\;}$K”ü+NaCl |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com