
| A. | 向 澄清石灰水通入过量CO2,先有白色沉淀后沉淀消失;则向澄清石灰水通入过量SO2,也是先有白色沉淀后沉淀消失 | |
| B. | ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 | |
| C. | 晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子 | |
| D. | 干冰(CO2)是分子晶体,则SiO2也是分子晶体 |
分析 A.澄清石灰水通入过量CO2,先生成碳酸钙后生成碳酸氢钙,澄清石灰水通入过量SO2,先生成亚硫酸钙后生成亚硫酸氢钙;
B.分子晶体的相对分子质量越大、沸点越大,含氢键的物质沸点较高;
C.金属晶体中含金属阳离子、自由电子;
D.SiO2由原子构成.
解答 解:A.澄清石灰水通入过量CO2,先生成碳酸钙后生成碳酸氢钙,澄清石灰水通入过量SO2,先生成亚硫酸钙后生成亚硫酸氢钙,CO2、SO2均为酸性氧化物,性质相似,可知类推合理,故A正确;
B.分子晶体的相对分子质量越大、沸点越大,含氢键的物质沸点较高,则ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4,而ⅤA族元素氢化物沸点顺序:NH3>AsH3>PH3,故B错误;
C.金属晶体中含金属阳离子、自由电子,不含阴离子,而含阴离子的一定为离子晶体,离子晶体含阴阳离子,故C错误;
D.SiO2由原子构成,为原子晶体,而干冰(CO2)是分子晶体,故D错误;
故选A.
点评 本题考查物质的性质,为高频考点,把握元素化合物知识、性质比较、氢键应用、晶体类型等为解答的关键,侧重分析与应用能力的考查,综合性较强,选项C为易错点,题目难度不大.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:选择题
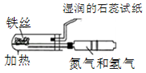 | 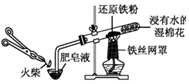 |
| A.模拟工业制氨气并检验产物 | B.一段时间后,试管中固体变为红棕色 |
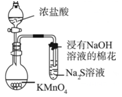 | 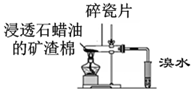 |
| C.可用所示装置比较KMnO4、Cl2、S的氧化性强弱 | D.若溴水褪色则证明石蜡油分解产生乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol CaC2中有3NA个离子 | |
| B. | 1mol SiO2中含有2NA个共价键 | |
| C. | 1L 1mol/L CH3COONa溶液中含NA个CH3COO-离子 | |
| D. | 42g C2H4和C3H6的混合物中一定含有6NA个氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu与Cl2直接化合生成CuCl2;Cu与S直接化合也能得到CuS | |
| B. | Fe3O4可写成FeO•Fe2O3;Pb3O4也可写成PbO•Pb2O3 | |
| C. | Mg失火不能用CO2灭火;Na失火也不能用CO2灭火 | |
| D. | 工业上电解熔融MgCl2制取金属镁;也用电解熔融AlCl3的方法制取金属铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
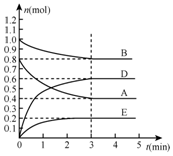 在某个容积为2L的密闭容器内,在T℃时按下图1所示发生反应:mA(g)+nB(g)?pC(g)+qE(s),△H<0(m、n、p、q为最简比例的整数).
在某个容积为2L的密闭容器内,在T℃时按下图1所示发生反应:mA(g)+nB(g)?pC(g)+qE(s),△H<0(m、n、p、q为最简比例的整数).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物 | |
| B. | 两种化合物组成元素相同,各元素质量分数也相同,则两者一定是同分异构体 | |
| C. | 相对分子质量相同的几种化合物,互称为同分异构体 | |
| D. | 组成元素的质量分数相同,且相对分子质量也相同的不同化合物,一定互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | xmol | B. | (x+0.1)mol | C. | 2xmol | D. | 0.1xmol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
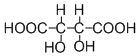
| A. | 酒精可以和水以任意比例互溶,与氢键有关 | |
| B. | 邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,与氢键有关 | |
| C. | 无机含氧酸的化学式可以用XOn(OH)m表示,n值越大,则该酸的酸性就越强.则可推知,硫酸酸性强于磷酸 | |
| D. | 如图该分子中没有手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲是苯的同系物,乙不是苯的同系物,甲乙瓦为同分异构体 | |
| B. | 甲、乙均能发生取代反应和加成反应 | |
| C. | 甲的一氯代物有2种,乙的一氯代物有7种(不考虑顺反异构) | |
| D. | 甲分子中所有原了可能在同一平面上,乙分子中所有原了一定在同一平面上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com