
【题目】Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( ) ![]()
A.MW6中各原子核外均满足8电子稳定结构
B.Q、W的单核离子的核外电子数相等
C.五种元素均能形成氢化物
D.W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强
 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示. 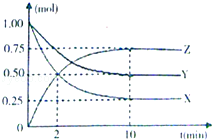
根据图中数据,完成下列问题:
(1)该反应的化学方程;
(2)反应开始至2min,气体Z的平均反应速率为;
(3)若X、Y、Z均为气体,则反应起始时与平衡后的压强之比是 .
(4)达到平衡后,下列说法不正确的是
A.X、Y、Z的浓度之比是1:2:3
B.X的消耗速率和Y的生成速率相等
C.Z的浓度保持不变
D.升高温度重新达到平衡,Z的浓度减小,则该反应为吸热反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程中,能量转化的主要方式不正确的是( )
A.硅太阳能电池工作时,光能转化成电能
B.铅蓄电池充电时,化学能转化成电能
C.电解质溶液导电时,电能转化成化学能
D.植物进行光合作用时,光能转化成化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g),CO2的平衡浓度c(CO2)与温度T的关系如图所示。下列说法错误的是

A. 反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的 ΔH>0
CO2(g)+H2(g)的 ΔH>0
B. 在T2时,若反应处于状态D,则一定有ν正>ν逆
C. 平衡状态A与C相比,平衡状态A的c(CO)大
D. 若T1、T2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是工业制取菱镁矿MgCO3(含杂质Al2O3、FeCO3)制取镁的工艺流程

请回答有关问题:
(1)菱镁矿进入酸浸池前需要粉碎,目的是 __________________________。
(2)氧化池通入Cl2的目的是氧化 _________________________(填化学式),工业上不选用硝酸做氧化剂的原因是_________________和_________________________。
(3)物质甲可以是_____________
A、MgO B、Mg(OH)2 C、NaOH溶液 D、稀氨水
(4)由MgCl2溶液制取无水MgCl2的操作方法 __________________________。
(5)当Fe3+完全沉淀时,求最小pH__________。已知:氢氧化铁ksp=1.0×10-38,离子浓度小于1×10-5 mol/L认为沉淀完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) ΔH1=-26.7 kJ·mol-1
②3Fe2O3(s)+CO(g)= 2Fe3O4(s)+CO2(g) ΔH2=-50.75 kJ·mol-1
③Fe3O4(s)+CO(g)= 3FeO(s)+CO2(g) ΔH3=-36.5 kJ·mol-1
则试通过计算判断,下列有关反应FeO(s)+CO(g)=Fe(s)+CO2(g)的能量变化示意图正确的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的密闭反应器中,只发生两个反应:a(g)+b(g) ![]() 2c(g) △H1<0; x(g)+3y(g)
2c(g) △H1<0; x(g)+3y(g) ![]() 2z (g) △H2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是
2z (g) △H2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是
A. 等压时,通入z气体,反应器中温度升高
B. 等容时,通入z气体,y的物质的量浓度增大
C. 等容时,通入惰性气体,各反应速率不变
D. 等压时,通入惰性气体,c的物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地.1mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( ) 
A.1 mol石墨完全转化为金刚石需吸收1.9 kJ的能量
B.石墨转化为金刚石属于物理变化
C.金刚石的稳定性强于石墨的
D.1 mol金刚石的能量大于1mol CO2的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com