

| 实验操作 | 实验现象 | |
| I | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为红棕色. |
| II | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化. |
| III | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(2013?西城区二模)下列实验操作不能达到预期实验目的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
(2013?西城区二模)对下列物质用途的解释不正确的是 ( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
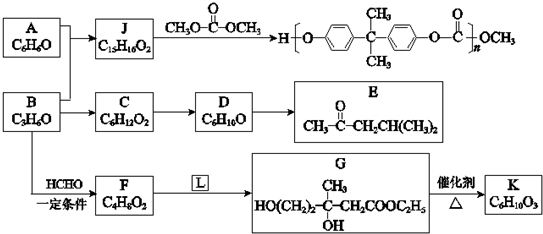
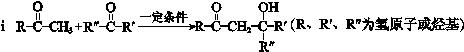

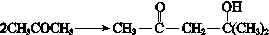
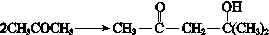
| △ |
| △ |
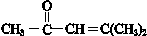
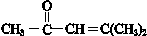
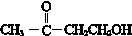
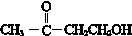
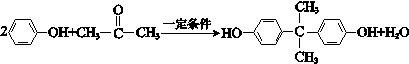

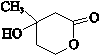

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com