
| 实验 | 操作 | |
| A | 除去NaHCO3固体中混有的NH4Cl | 直接将固体加热 |
| B | 实验室收集Cu与稀硝酸反应成的NO | 向上排空气法收集 |
| C | 检验乙酸具有酸性 | 配制乙酸溶液,滴加NaHCO3溶液有气泡产生 |
| D | 测定某稀硫酸的浓度 | 取20.00ml该稀硫酸于干净的锥形瓶中,用 0.1000mol/L的NaOH标准液进行滴定 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碳酸氢钠热稳定性较弱,加热易分解生成碳酸钠、二氧化碳和水;
B.NO与空气中氧气反应,不能用排空气法收集;
C.乙酸溶液中滴加NaHCO3溶液有气泡产生,证明乙酸的酸性大于碳酸;
D.该中和滴定实验中没有加入指示剂.
解答 解:A.由于碳酸氢钠加热易分解,不能利用加热的方法除去NaHCO3固体中混有的NH4Cl,故A错误;
B.NO与氧气反应,应该用排水法收集,不能用排空气法收集,故B错误;
C.配制乙酸溶液,滴加NaHCO3溶液有气泡产生,证明乙酸的酸性大于碳酸,碳酸具有酸性,则证明乙酸具有酸性,故C正确;
D.稀硫酸与NaOH溶液的反应没有明显现象,需要滴入指示剂,否则无法完成实验,故D错误;
故选C.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及物质分离与提纯、气体收集方法、中和滴定等知识,明确常见化学实验基本操作方法为解答关键,试题培养了学生的分析能力及化学实验能力.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:选择题

| A. | 该装置的能量转化方式为太阳能转化为电能 | |
| B. | 工作时,阳极附近pH减小 | |
| C. | 电路中每转移4mol电子,捕获44g二氧化碳 | |
| D. | 阴极的电极反应为CO2+2e-=CO+O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质都能发生水解反应 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 苯不能使溴的四氯化碳溶液褪色,但能与H2发生加成反应 | |
| D. | 因分子中均含有官能团“-OH”,故乙醇、乙酸水溶液均呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键 | |
| B. | 水分子是一种极性分子,水分子空间结构呈直线型 | |
| C. | 冰与干冰都是分子晶体,其晶胞中分子的空间排列方式类似 | |
| D. | 水分子间通过H-O键形成冰晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
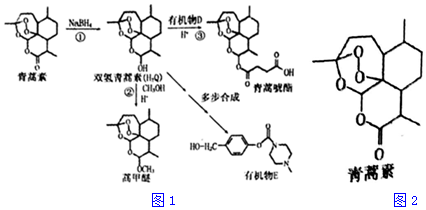
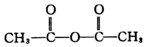 +H-OH→
+H-OH→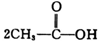
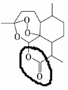 ;根据酯的性质判断青蒿素可能具有的某种化学性质和反应条件为可在酸性或碱性条件下发生水解反应.屠呦呦教授率领的研究团队先后经历了用水、乙醇、乙醚提取青蒿素的探究过程,最终确认只有采用低温、乙醚冷浸等方法才能成功提取青蒿素;研究发现这是因为青蒿素分子中的某个基团在提取过程中对热不稳定,试写出该基团的结构式-O-O-.
;根据酯的性质判断青蒿素可能具有的某种化学性质和反应条件为可在酸性或碱性条件下发生水解反应.屠呦呦教授率领的研究团队先后经历了用水、乙醇、乙醚提取青蒿素的探究过程,最终确认只有采用低温、乙醚冷浸等方法才能成功提取青蒿素;研究发现这是因为青蒿素分子中的某个基团在提取过程中对热不稳定,试写出该基团的结构式-O-O-.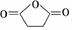 .
.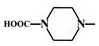 外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式
外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式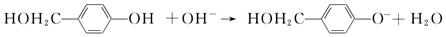 ,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有3种.
,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有3种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
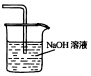 | 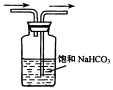 | 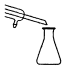 |  |
| 尾气吸收Cl2 | 吸收CO2中的HCl杂质 | 蒸馏时的接收装置 | 乙酸乙酯的收集装置 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W、M的离子半径为M<W | |
| B. | YZ2为直线形的共价化合物,W2Z2既含有离子键又含有共价键 | |
| C. | Z与X形成的化合物的熔沸点偏高是因其分子内存在氢键 | |
| D. | Z与M形成的化合物可作为耐高温材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3能中和胃酸,对胃壁不产生强烈的刺激或腐蚀作用,可用于治疗胃酸过多症,但不适合胃溃疡病人 | |
| B. | NaHCO3能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头 | |
| C. | 可以用澄清石灰水来鉴别Na2CO3溶液中和NaHCO3溶液 | |
| D. | 往Na2CO3饱和溶液中通入CO2气体,可获得NaHCO3沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com