
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.元素X与氢形成原子个数比为1:1的化合物有多种 |
| B.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
| C.Z的原子半径比Y的原子半径大 |
| D.元素Z可与元素X形成共价化合物XZ2,且各微粒均满足8电子的稳定结构 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径: T> W > Z > Y |
| B.W与T的单质可通过电解饱和的WT水溶液获得 |
| C.Z与W形成的两种化合物中化学键类型完全相同 |
| D.元素X、Z与T可形成多种酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.比较这两种元素的单质的密度和熔点 |
| B.在氯化铝和氯化镁的溶液中分别滴加过量的氨水 |
| C.将空气中久置的镁带和铝片分别置于热水中,并滴入酚酞溶液 |
| D.用pH计分别测量相同物质的量浓度的氯化铝溶液和氯化镁溶液的pH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Z与M形成的化合物中不可能含有非极性键 |
| B.对应氢化物的热稳定性:X > Y >M |
| C.单质的还原性:R> M>Y>X |
| D.X、Y、M、Z 4种元素组成的离子化合物受热易分解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A | | B | C |
| | | D | E |
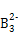 、A2
、A2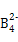
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | | X | |
| Y | Z | | W |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com