
化合物C是制备液晶材料的中间体之一,它可由A和B在一定条件下制得
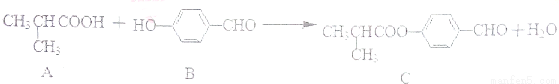
下列说法正确的是
A.每个A分子中含有1个手性碳原子
B.可以用酸性KMnO4溶液检验B中是否含有醛基
C.B、C各1mol分别和氢气反应,最多消耗氢气均为4molH2
D.C可发生加成反应、取代反应、氧化反应等
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年江西省等四校高二下第二次月考化学试卷(解析版) 题型:选择题
中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用。有机物M是中药狼把草的成分之一,其结构如图所示。下列叙述不正确的是( )

A.M是芳香族化合物,它的分子式为C9H5O4Cl
B.1 mol M最多能与含2 mol Br2的溴水发生反应
C.1 mol M分别与足量的NaOH溶液、Na2CO3溶液反应,消耗两种物质的物质的量分别为4 mol、2mol
D.在一定条件下能发生取代、加成、水解、氧化等反应
查看答案和解析>>
科目:高中化学 来源:2016届陕西西藏民族学院附中高三下考前三模理综化学试卷(解析版) 题型:实验题
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业.CuCl 难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu 和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl 的工艺过程如下:
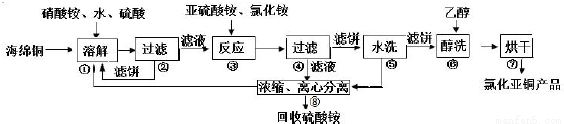
回答下列问题:
(1)步骤①中真正的氧化剂是___________,溶解温度应控制在60-70 度,原因是___________;
(2)写出步骤③中主要反应的离子方程式是___________;
(3)步骤⑧是分离滤液和洗涤液操作,实验室里混有杂质NaCl 的(NH4)2SO4 固体提纯的方法是___________;
(4)上述工艺中,步骤⑥不能省略,理由是___________;
(5)步骤②、④、⑤、⑧都要进行固液分离.工业上常用的固液分离设备有___________(填字母).
A、离心机B、分馏塔C、框式压滤机D、反应釜
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3 溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L 的K2Cr2O7 溶液滴定到终点,消耗K2Cr2O7 溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl 的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮复习训练六化学试卷(解析版) 题型:选择题
某化学小组在常温下测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案,下列有关判断中不正确的是( )
方案Ⅰ:铜铝混合物 测定生成气体的体积;方案Ⅱ:铜铝混合物
测定生成气体的体积;方案Ⅱ:铜铝混合物 测定剩余固体的质量
测定剩余固体的质量
A.溶液A和B均可以是盐酸或NaOH溶液
B.溶液A和B不可以均选用稀硝酸
C.若溶液B选用浓硝酸,则测得铜的质量分数偏大
D.实验室方案Ⅱ更便于实施
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前周练模拟化学试卷(解析版) 题型:填空题
化合物H是合成治疗高血压药物奈必洛尔的重要中间体,其部分合成路线图如下(Ph代表苯基):

(1)化合物C的含氧官能团名称为________、________。
(2)B→C的反应类型是________。
(3)写出A→B的化学反应方程式________。
(4)C→D的转化中,反应物G的分子式为C6H10O3,生成物除D外还有Ph3P=O,则G的结构简式为_________
(5)写出同时满足下列条件的B的一种同分异构体的结构简式________。
Ⅰ.分子中含有一个酯基和一个手性碳原子,有4种化学环境不同的氢;
Ⅱ.不能发生银镜反应;
Ⅲ.能发生水解反应,且其中一种水解产物能与FeCl3溶液发生显色反应。
(6)已知:
①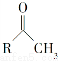
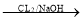 RCOONa
RCOONa
②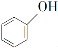
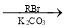
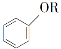
化合物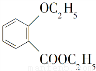 是一种重要的有机合成中间体,请写出以苯酚、乙醇和
是一种重要的有机合成中间体,请写出以苯酚、乙醇和 为原料制备该化合物的合成路线流程图(无机试剂作用)。合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂作用)。合成路线流程图示例如下:
H2C===CH2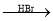 CH3CH2Br
CH3CH2Br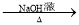 CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前周练模拟化学试卷(解析版) 题型:选择题
短周期元素W、Y、Z的原子序数依次增大,W与Y最外层电子数之和为X的最外层电子数的2倍。Z最外层电子数等于最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体,下列说法正确的是
A.离子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z)
B.W的气态氢化物比X的稳定
C.XY2与ZY2中的化学键类型相同
D.Y的最高价氧化物对应水化物的酸性比W的强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北市高一5月月考化学试卷(解析版) 题型:填空题
向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)?SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示;
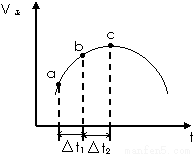
(1)点a-c段,速率变化的主要原因是_______________,点c后速率变化的主要原因是____________;
(2)c点是否已经达到平衡状态_______(填“是”、“否”或“不一定”);
(3)反应物浓度:a点_______b点(填“<”、“=”或“>”);
(4)反应物的总能量_______生成物的总能量(填“<”、“=”或“>”);
(5)△t1=△t2时,SO2物质的量的变化量:a~b段_______b~c段(填“<”、“=”或“>”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北市高一5月月考化学试卷(解析版) 题型:选择题
100mL浓度为2mol•L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是
A.加入适量的6mol/L的盐酸 B.加入数滴氯化铜溶液
C.加入适量蒸馏水 D.加入适量的氯化钠溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学孔德校区高二下6月考化学卷(解析版) 题型:填空题
下列几组物质中,互为同位素的有__________,互为同素异形体的有________,互为同系物的有____________,互为同分异构体的有___________,属于同种物质的有__________。
①O2和O3 ②CH3CH2CH2CH(C2H5)CH3 和 CH3CH2CH2CH(CH3)C2H5
③H、D、T ④ CH3CH2CH2CH3 和(CH3)2CHCH3 ⑤乙烷和丁烷⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com