
| A、镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| B、铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
| C、铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| D、在潮湿的碱性环境中,金属的电化学腐蚀主要是析氢腐蚀 |


科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液体积(ml) | 标准盐酸体积(ml) | |
| 滴定前刻度(ml) | 滴定后刻度(ml) | ||
| 第一次 | 10.00 | 0.20 | 20.50 |
| 第二次 | 10.00 | 0.40 | 20.80 |
| 第三次 | 10.00 | 4.00 | 24.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 常温下状态 | 溶解性 | 稳定性 |
| 白色固体 | 易溶于水和乙醇,难溶于CCl4 | 在干燥空气中稳定,在湿空气中放出氨转化为NH4HC03,59时分解为NH3和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、NO3ˉ、Fe2+、Clˉ |
| B、SO42-、Mg2+、Clˉ、Na+ |
| C、SO42-、Na+、Mg2+、CH3COOˉ |
| D、Clˉ、SCNˉ、K+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:16 | B、16:1 |
| C、17:7 | D、7:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 用图能证明酸性:硫酸>碳酸>次氯酸 |
B、 用图所示装置分离出溴苯 |
C、 用图设计成铜锌原电池装置 |
D、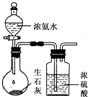 用图制取干燥的氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com