
分析 (1)依据化学反应速率之比等于系数之比计算得到;
(2)①2SO2(g)+O2═2SO3(g)△H=-196.6kJ•mol-1,
②2NO(g)+O2═2NO2(g)△H=-113.0kJ•mol-1.
根据盖斯定律可知:将$\frac{①-②}{2}$计算;
(3)根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:(1)反应的化学方程式为:2SO2(g)+O2(g)?2SO3(g),反应速率之比等于系数之比,v(SO2):v(O2):v(SO3)=2:1:2,反应速率υ(SO2)为0.05mol•L-1•min-1,依据比例计算得到v(O2)=0.025mol/L•min;v(SO3)=0.05mol•L-1•min-1,
故答案为:0.025 mol•L-1•min-1; 0.05 mol•L-1•min-1;
(2)已知:①2SO2(g)+O2═2SO3(g)△H=-196.6kJ•mol-1,
②2NO(g)+O2═2NO2(g)△H=-113.0kJ•mol-1.
根据盖斯定律可知:将$\frac{①-②}{2}$可得:NO2(g)+SO2(g)═SO3(g)+NO(g)△H=$\frac{-196.6+113}{2}$=-41.8 kJ•mol-1,
故答案为:-41.8;
(3)a、反应前后气体两边的计量数相等,所以体系压强始终不变,故错误;
b、混合气体颜色保持不变,则二氧化氮的浓度不变,正逆反应速率相等,说明达平衡状态,故正确;
c、三氧化硫和一氧化氮的体积比始终是1:1,无法判断是否达到了平衡状态,故错误;
d、每消耗1mol SO3等效于消耗1mol NO同时生成1mol NO,正逆反应速率相等,达平衡状态,故正确;
故选:b、d.
点评 本题考查了物质反应过程中的能量变化分析判断、化学平衡状态的判断和盖斯定律的应用,化学反应速率的计算应用,题目难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
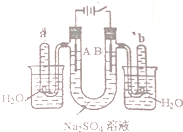 如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液.下列有关叙述正确的是( )
如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液.下列有关叙述正确的是( )| A. | 逸出气体的体积,A电极的小于B电极的 | |
| B. | 一电极逸出无味气体,另一电极逸出刺激性气味气体 | |
| C. | A电极附近呈红色,B电极附近呈蓝色 | |
| D. | 电解一段时间后,将全部电解液转移到同一烧杯中,充分搅拌后溶解呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气象环境报告中的“PM2.5”是对一种新分子的描述 | |
| B. | 长期使用硫酸铵(NH4)2SO4化肥会使土壤酸化 | |
| C. | “玉兔号”月球车太阳能电池帆板的材料是二氧化硅 | |
| D. | 高铁车厢采用的铝合金材料强度大、质量轻,不与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
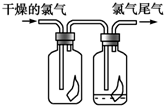 (1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.
(1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHS 溶于水:NaHS═Na++HS- HS-?H++S2- | |
| B. | (NH4)2SO4溶于水:(NH4)2SO4?2NH4++SO42- | |
| C. | 磷酸溶于水中:H3PO4═3H++PO43- | |
| D. | Al(OH)3的电离:Al(OH)3=Al3++3OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与硫酸铜溶液反应:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ | |
| B. | 向10mL1mol/LNa2CO3溶液中逐滴加入5mL1mol/L盐酸:2H++CO${\;}_{3}^{2-}$═CO2↑+H2O | |
| C. | 将过量SO2通入冷氨水中:SO2+NH3•H2O═HSO${\;}_{3}^{-}$+NH${\;}_{4}^{+}$ | |
| D. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO${\;}_{3}^{-}$═Ag++NO↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关.回答下列问题:
碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com