
| 选项 | 实验操作和现象 | 结论 |
| A | 分别测定饱和NaClO溶液与饱和CH3COONa溶液的pH,pH(NaC1O)>pH(CH3COONa) | ClO-结合H+的能力比 CH3COO- 的强 |
| B | 25℃时,向pH等于2的醋酸溶液中加入少量0.0lmol•L-1的稀盐酸,溶液的pH会变小 | 醋酸的电离程度增大 |
| C | 将稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 氧化性:H2O2>Fe3+ |
| D | 向2mL2%NaOH溶液中加入lmLl%CuSO4溶液,振荡后滴加0.5mL5%葡萄糖溶液,加热至沸腾,出现红色沉淀 | 葡萄糖中含有醛基 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.饱和NaClO溶液与饱和CH3COONa溶液的浓度不同;
B.加入少量0.0lmol•L-1的稀盐酸,氢离子浓度增大,醋酸电离平衡的逆向移动;
C.过氧化氢、硝酸根离子均可氧化亚铁离子;
D.碱性条件下,葡萄糖与氢氧化铜反应生成砖红色沉淀.
解答 解:A.饱和NaClO溶液与饱和CH3COONa溶液的浓度不同,应测定等浓度时盐溶液的pH比较酸性,故A错误;
B.加入少量0.0lmol•L-1的稀盐酸,氢离子浓度增大,抑制醋酸的电离,说明醋酸电离平衡逆向移动,电离程度减小,故B错误;
C.过氧化氢、硝酸根离子均可氧化亚铁离子,则不能说明氧化性:H2O2>Fe3+,故C错误;
D.碱性条件下,葡萄糖与氢氧化铜反应生成砖红色沉淀,则葡萄糖中含有醛基,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、盐类水解、有机物的检验等为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 | |
| B. | 工业上,电解熔融MgCl2制金属镁 | |
| C. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| D. | “冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为10 的氧原子:10O | |
| B. | 过氧化氢的电子式:H-O-O-H | |
| C. | CS2中各原子最外层都满足8 电子结构 | |
| D. | CH2Cl2是四面体构型的含非极性健的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②>④>③>① | B. | ①>②>④>③ | C. | ①>②>③>④ | D. | ③>②>④>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12 | B. | 11 | C. | 4 | D. | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为8的氮原子:${\;}_{8}^{15}$N | B. | 乙醇的实验式:C2H6O | ||
| C. | 氯化镁的电子式: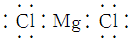 | D. | 硫原子的结构示意图: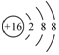 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF比H2O稳定性更强,是由于HF分子间作用力较大 | |
| B. | CC14、N2和SiO2晶体中,各原子最外层都达到8电子稳定结构 | |
| C. | Na投入到水中,有共价键的断裂与形成 | |
| D. | 离子化合物中一定含有离子键,可能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 有机物 | 水杨酸 | 冬青油 | 阿司匹林 |
结构简式 |  |  | 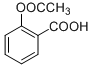 |
| A. | 可以用FeCl3溶液鉴别冬青油和阿司匹林 | |
| B. | 由水杨酸制冬青油的反应是取代反应 | |
| C. | 1mol阿司匹林最多能与3 mol NaOH反应 | |
| D. | 可以用碳酸钠溶液除去冬青油中少量的水杨酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因 | |
| B. | 人造纤维、合成纤维和光导纤维都是有机离分子化合物 | |
| C. | 纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 | |
| D. | 可用Si2N4、Al2O3制作高温结构陶瓷制品 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com