
| A. | 定性检验C2H5Cl中的氯元素:将C2H5Cl和NaOH溶液混合加热后,再加AgNO3溶液 | |
| B. | 检验汽油是否含有烯烃:取少量汽油,加入碘酒,振荡并观察 | |
| C. | 制乙烯:将无水乙醇加热到170℃ | |
| D. | 蛋白质变性实验:将硫酸铜溶液滴入鸡蛋清溶液中 |
分析 A.在加硝酸银溶液制取必须先加稀硝酸中和未反应的碱;
B.烯烃和炔烃都能和碘发生加成反应;
C.在浓硫酸作催化剂、加热到170℃下用无水乙醇制取乙烯;
D.重金属盐能使蛋白质发生变性.
解答 解:A.在加硝酸银溶液制取必须先加稀硝酸中和未反应的碱,否则硝酸银和NaOH反应而影响实验,故A错误;
B.烯烃和炔烃都能和碘发生加成反应,所以不能用碘酒检验汽油中是否含有烯烃,故B错误;
C.在浓硫酸作催化剂、加热到170℃下用无水乙醇制取乙烯,需要浓硫酸作催化剂,故C错误;
D.重金属盐能使蛋白质发生变性,硫酸铜是重金属盐,能使蛋白质变性,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及物质制备、物质检验,明确实验原理及物质性质是解本题关键,注意从实验操作规范性、试剂滴加顺序分析解答,物质检验时要排除其它物质的干扰,易错选项是A.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:解答题
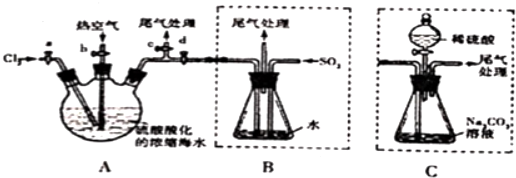
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60% | B. | 33.3% | C. | 36% | D. | 40% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | 只有⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
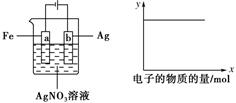
| A. | ①②⑤ | B. | ③④ | C. | ①②④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
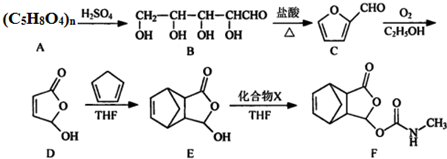
 .
.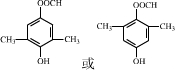 .
.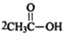 $\stackrel{P_{2}O_{3}}{→}$
$\stackrel{P_{2}O_{3}}{→}$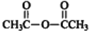 ,化合物
,化合物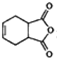 是合成抗病毒药阿普洛韦的中间体,请设计合理方案以
是合成抗病毒药阿普洛韦的中间体,请设计合理方案以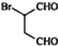 和
和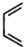 为原料合成该化合物(用合成路线流程图表示:并注明反应条件).合成路线流程图实力如下CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2$\stackrel{Br_{2}}{→}$
为原料合成该化合物(用合成路线流程图表示:并注明反应条件).合成路线流程图实力如下CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2$\stackrel{Br_{2}}{→}$
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸氢钠稀溶液 | B. | 硝酸钠溶液 | C. | 醋酸钠溶液 | D. | 硫酸铜溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com