
 +2CH2=C(CH3)2→
+2CH2=C(CH3)2→ +CH2=CH.
+CH2=CH. 分析 (1)当条件不足时,根据碳原子和氢原子个数为正整数并且所含有的某原子的质量分数为讨论依据,结合相对分子质量小于200可以得出有机物的分子式或某种原子的个数,据此解答即可;
(2)依据反应特点确定反应类型,依据反应物与生成物书写离子反应方程式.
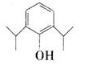
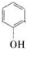
解答 解:(1)芳香族含氧衍生物中氧的质量分数约为9%,设氧原子个数为n(为整数),则$\frac{16n}{9%}$<200,解得n=1,所以有机物的相对分子质量M=$\frac{16}{9%}$≈178,178-16=162,$\frac{162}{14}$≈12,依据题意得出该有机物能与FeCl3发生显色反应,故一定含有酚羟基,即一定含有苯环,有机物中最多也只能含有12个碳原子(因为如果是12个碳时,加上一个氧原子,相对分子质量已经是160),剩余18个H,正好符合苯的同系物通式,故此有机物的分子式为:C12H18O,此有机物含有苯环和酚羟基,分子中含有三个相邻且对称的取代基或官能团,取代基上一氯代物有两种,故另外的两个烷烃基为:-C3H7,即丙基,依据此有机物的名称得知:为异丙酚,故此丙基为异丙基,故结构简式为: ,故答案为:C12H18O;
,故答案为:C12H18O; ;
;
(2)只含一个甲基的单烯烃A即为丙烯,丙烯与苯酚反应生成异丙酚属于加成反应,即丙烯中碳碳双键断开,分别加成苯酚基和H原子,只含一个支链的最简单烯烃为:2-甲基-1-丙烯,对苯酚进行烷基化反应生成异丙酚,化学反应方程式为: +2CH2=C(CH3)2→
+2CH2=C(CH3)2→ +CH2=CH2,故答案为:
+CH2=CH2,故答案为: +2CH2=C(CH3)2→
+2CH2=C(CH3)2→ +CH2=CH.
+CH2=CH.
点评 本题主要考查的是有机物分子式以及结构简式的确定,本题还涉及有机化学反应类型的判断、有机化学反应方程式的书写,有一定难度.


科目:高中化学 来源: 题型:解答题
 2014年3.15晚会的主题为“让消费更有尊严”,食品行业依旧是消费者最为关注的行业.频发的食品安全事件,让公众几乎患上了“食物焦虑症”.国际环保组织绿色和平发布报告,称对“立顿”的绿茶、茉莉花茶和铁观音袋泡茶检验,发现含有被国家禁止在茶叶上使用的高毒农药灭多威.灭多威是一种白色晶状固体,略具有硫磺的气味,其化学式为C5H10N2O2S.
2014年3.15晚会的主题为“让消费更有尊严”,食品行业依旧是消费者最为关注的行业.频发的食品安全事件,让公众几乎患上了“食物焦虑症”.国际环保组织绿色和平发布报告,称对“立顿”的绿茶、茉莉花茶和铁观音袋泡茶检验,发现含有被国家禁止在茶叶上使用的高毒农药灭多威.灭多威是一种白色晶状固体,略具有硫磺的气味,其化学式为C5H10N2O2S.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 自从1962年首次合成了第一个稀有气体的化合物XePtF6以来,人们又相继发现了氙气的一系列化合物如XeF2、XeF4等.巴特列为开拓稀有气体化学作出了历史性贡献.
自从1962年首次合成了第一个稀有气体的化合物XePtF6以来,人们又相继发现了氙气的一系列化合物如XeF2、XeF4等.巴特列为开拓稀有气体化学作出了历史性贡献.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的中子数 | B. | 13C与C60互为同位素 | ||
| C. | 15N与14N互为同位素 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1moL苯乙烯(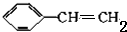 )中含有的碳酸双键数为4NA )中含有的碳酸双键数为4NA | |
| B. | 加热条件下,4.6g金属Na与足量O2反应的产物中阴离子的数目为0.1NA | |
| C. | 室温条件下,pH=9,体积为1L的CH4COONa溶液中,发生电离的水分子数为1.0×10-4NA | |
| D. | 高温条件下,16.6g铁粉与足量水蒸气反应后,转移电子数为0.9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+)=c(K+)=c(Ba2+) | |
| B. | 将10mL0.1mol•L-1Na2CO3溶液逐滴滴加到10mL0.1mol•L-1盐酸中:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-) | |
| C. | 向NH4HCO3溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)=c(HCO3-)+c(CO32-) | |
| D. | 0.2mol•L-1的某一元弱酸HA溶液和0.1mol•L-1NaOH溶液等体积混合后的溶液:2c(OH-)+c(A-)=2c(H+)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 甲 | 乙 | 丙 | 实验结论 |  |
| A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:碳>硅 | |
| B | 双氧水 | MnO2 | Na2S | 氧化性:H2O2>O2>S | |
| C | 浓硫酸 | Na2SO3 | 酸性KMnO4溶液 | SO2具有漂白性 | |
| D | 浓氨水 | 氢氧化钠固体 | 酚酞 | 碱性:NaOH>NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
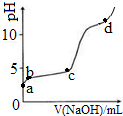 室温下,在0.2mol/LAl2(SO4)3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列说法正确的是( )
室温下,在0.2mol/LAl2(SO4)3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列说法正确的是( )| A. | a点,离子方程式为:Al3++3OH-→Al(OH)3↓ | |
| B. | a~b段,溶液pH增大,促进了氢氧化铝的碱式电离 | |
| C. | b~c段,加入的OH-主要用于生成Al(OH)3沉淀 | |
| D. | d点时,Al(OH)3沉淀开始溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com