
【题目】X、Y、L、M、R、Q是短周期主族元素,部分信息如下表所示:
X | Y | Z | M | R | Q | |
原子半径 | 0.186 | 0.074 | 0.099 | 0.143 | ||
主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
其他 | 阳离子无核外电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(1)X和M的原子可构成18电子的分子,该分子的结构式为_______ .
(2)Z与Q相比,金属性较强的是_______ (用元素符号表示),下列事实能证明一结论的是_______ (填字母序号)。
a.Q的熔点比Z的熔点高,Q的硬度比Z的硬度大
b.Z与冷水反应迅速,而Q与冷水几乎不反应
c.Z的最高价氧化物对应水化物是强碱,而Q的最高价氧化物对应水化物具有两性
(3)与Y元素同主族的短周期元素E在自然界中存在多种核素,它们之间的关系互为_______,其中用于测定一些文物年代的核素的符号为_______ 。
(4)写出Z2M2的电子式:_______。
【答案】 H—O—O—H Na b c 同位素 ![]()
![]()
【解析】X、Y、Z、M、R、Q是短周期主族元素,X阳离子核外无电子,则X为H元素;Y有+4、-4价,是无机非金属材料的主角,则Y为Si;Z焰色反应呈黄色,则Z为Na;M只有-2价,则为O元素;R有+7、-1价,则R为Cl;Q有+3,原子半径大于Cl,则Q为Al。
(1)H和O的原子可构成18电子的分子为过氧化氢,该分子的结构式为H—O—O—H,正确答案: H—O—O—H。
(2) Na与Al相比较,Na的金属性较强,比较金属性,可根据与水反应的剧烈程度以及对应的最高价氧化物的水化物的碱性强弱判断,碱性越强,对应的元素的金属性越强;而与单质的熔沸点、硬度与判断元素金属性无关,b c正确;正确答案:Na; b c。
(3)Y元素为硅,与硅同主族的元素为碳,同种元素的不同核素互称同位素,其中用于测定一些文物年代的核素的符号为![]() ;正确答案:同位素 ;
;正确答案:同位素 ; ![]() 。
。
(4)元素Z为钠,元素M为氧,二种元素组成a2O2,它为离子化合物,电子式为![]() ;正确答案:
;正确答案:![]() 。
。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】硫酸钾和硫酸铝的混合溶液,已知其中Al3+的浓度为0.4 mol·L-1,硫酸根离子浓度为0.7 mol·L-1,则K+的物质的量浓度为 ( )
A. 0.1 mol·L-1 B. 0.15 mol·L-1 C. 0.3 mol·L-1 D. 0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,A、B、C、D、E是长式元素周期表中的5种元素(不包括镧系和锕系)。下列说法不正确的是

A. D、E 原子序数之差可能是8、18或32 B. B、C原子序数之差一定是2
C. A、E 原子序数之差可能为2 D. B、D原子序数之差不可能是7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程与能量的说法中正确的是( )
A.中和反应是吸热反应
B.燃烧属于放热反应
C.化学键断裂放出能量
D.吸热反应中,反应物总能量大于生成物总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的四种元素,A2﹣和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
(1)四种元素中电负性最大的是(填元素符号),其中C原子的核外电子排布式为 .
(2)单质A有两种同素异形体,其中沸点高的是(填分子式),原因是;A和B的氢化物所属的晶体类型分别为和 .
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为 , 中心原子的杂化轨道类型 .
(4)化合物D2A的立体构型为 , 中心原子的价层电子对数为 , 单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为 .
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为 , 晶胞中A原子的配位数为;列式计算晶体F的密度(gcm﹣3).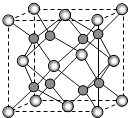
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】8g NaOH固体溶于水配成1000 mL溶液,取出其中的10 mL,该10 mL NaOH溶液的物质的量浓度为 ( )
A. 1 molL-1 B. 0.5 molL-1 C. 0.25 molL-1 D. 0.2 molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,2体积气体A2和1体积气体B2完全反应生成了2体积气体X,则X的化学式是( )
A. A2BB. A2B2C. AB2D. AB3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验事实得出的结论正确的是( )
A.由SiO2不能与水反应生成H2SiO3 , 可知SiO2不是H2SiO3的酸酐
B.由SiO2+2C ![]() Si+2CO↑,可知碳的非金属性大于硅
Si+2CO↑,可知碳的非金属性大于硅
C.CO2通入Na2SiO3溶液产生白色沉淀,可知酸性H2CO3>H2SiO3
D.SiO2可与NaOH溶液反应,也可与氢氟酸反应,可知SiO2为两性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com