
| A. | ${\;}_{6}^{12}$C与${\;}_{6}^{14}$C互为同位素 | B. | 乙烯分子的结构简式:CH2=CH2 | ||
| C. | 氟离子结构示意图: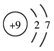 | D. | -OH的电子式: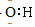 |
分析 A.同位素是质子数相同中子数不同的同种元素的不同原子;
B.乙烯分子中含有碳碳双键官能团;
C.氟离子的核电荷数为9、核外电子数为10;
D.羟基是中性原子团,氧原子有一个成单电子.
解答 解:A.${\;}_{6}^{12}$C与${\;}_{6}^{14}$C质子数相同中子数不同为碳元素的同位素互为同位素,故A正确;
B.乙烯分子中含碳碳双键,乙烯的结构简式:CH2=CH2 ,故B正确;
C.氟离子得到了1个电子,核外电子水为10,氟离子结构示意图为: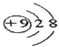 ,故C错误;
,故C错误;
D.羟基是中性原子团,氧原子有一个成单电子,-OH的电子式: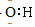 ,故D正确;
,故D正确;
故选C.
点评 本题考查常见化学用语的正误判断,题目难度中等,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,该类试题需要明确的是常见的化学用语主要包括元素符号、化学式、化合价、电子式、原子结构示意图、结构式、结构简式以及方程式和各种模型等,需要学生熟练记住.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 80g硝酸铵中含有氮原子数为NA | |
| B. | 0.lmolN5+离子中所含的电子数为3.4 NA | |
| C. | 2mol金属铝与足量的盐酸反应,共失去了4NA个电子 | |
| D. | 16 g氧气和16 g臭氧所含的原子数均为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL质量分数为98%的H2SO4用10mL水稀释后;H2SO4的质量分数大于49% | |
| B. | 在标准状况下,将11.2 L氨气溶于500mL水中,得到1mol•L-1的氨水 | |
| C. | 配制0.1 mol•L-1的Na2CO3溶液480mL,需用500ml容量瓶 | |
| D. | 向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取CuSO4:Cu$\stackrel{浓H_{2}SO_{4}、△}{→}$CuSO4 | |
| B. | 制取Cu(NO3)2:Cu$\stackrel{O_{2}、△}{→}$ $\stackrel{HNO_{3}}{→}$Cu(NO3)2 | |
| C. | 制取Al(OH)3:Al$\stackrel{NaOH}{→}$ $\stackrel{H_{2}SO_{4}}{→}$Al(OH)3 | |
| D. | 制取Na2CO3:Na$\stackrel{O_{2}}{→}$ $\stackrel{CO_{2}}{→}$Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Na、K | B. | Na、Mg、Al | C. | Li、Be、Mg | D. | Li、Na、Mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com