
| A. | KClO3→HCl | B. | Na2O2→O2 | C. | Fe Cl3→FeCl2 | D. | SO2→SO3 |
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲基电子数为10NA | |
| B. | 26 g乙炔所含共用电子对数目为3 NA | |
| C. | 标准状况下,11.2 L CCl4所含分子数为0.5 NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与乙醇反应时增大乙醇的用量 | |
| B. | 实验室制CO2气体时,将大理石块改为大理石粉 | |
| C. | 溴水与KI溶液反应时增大压强 | |
| D. | 铝与稀硫酸反应制取氢气时改用浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 表示6种核素 | |
| B. | ${\;}_{3}^{6}$Li和${\;}_{3}^{7}$Li为同种元素的不同核素,互称同位素 | |
| C. | ${\;}_{6}^{14}$C和${\;}_{7}^{14}$N质量数相同,属于同主族元素 | |
| D. | ${\;}_{11}^{23}$Na和${\;}_{12}^{24}$Mg的中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 装置 | 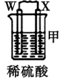 |  | 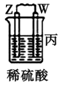 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A. | 装置甲中X电极附近有气泡产生 | |
| B. | 装置乙中Y电极上的反应式为Cu2++2e-=Cu | |
| C. | 装置丙中溶液的pH增大 | |
| D. | 四种金属的活动性强弱顺序为W>X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液漏斗从食醋中分离出乙酸 | |
| B. | 用硫氰化钾溶液检验FeCl2溶液是否变质 | |
| C. | 用氢氧化钠溶液除去Cl2中含有的少量HCl | |
| D. | 用硝酸银溶液鉴别Na2SO4和Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题


| A. | 已知过程①的产物还有H2和B(OH) 4-,则反应的离子方程式是2Fe2++BH4-+4OH-=2Fe+2H2↑+B(OH) 4- | |
| B. | 过程②的离子方程式为4Fe+NO3-+10H+=4Fe2++NH4++3H2O | |
| C. | 研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是纳米铁粉与H+反应生成H2 | |
| D. | 相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异(见图),产生该差异的可能原因是离子浓度越大,反应速率越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③⑤ | C. | ②③④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 78g Na2O2中含有的离子总数为4NA | |
| B. | 标准状况下,1.12L HF中所含的分子总数为0.05NA | |
| C. | 由CO2和O2组成的混合物共有NA个分子,其中的氧原子数为2NA | |
| D. | 0.11mol•L-1 FeCl3溶液中含有的Cl-数目为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com