
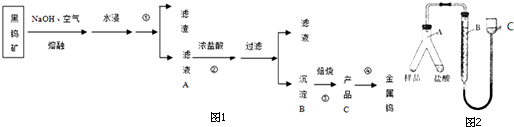
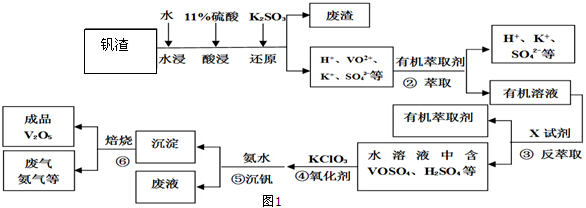
分析 黑钨矿碱溶后,得到得到的滤液为钨酸的钠盐,加入浓盐酸,制取钨酸;钨酸(H2WO4)加热分解产生三氧化钨(WO3),判断C为三氧化钨(WO3);H2、CO等还原氧化钨生成钨;
(1)根据化合价升降分析氧化还原反应;
(2)操作①之后,分为滤渣和滤液,故为过滤;钨酸钠和浓盐酸反应生成钨酸(H2WO4)和氯化钠;钨酸(H2WO4)加热分解产生三氧化钨(WO3)和水,判断C为三氧化钨(WO3);H2、CO还原氧化钨生成钨;
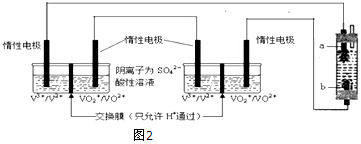
(3)为测定其中金属钨的含量(已知金属钨不溶于盐酸),首先检验检查气密性;然后加入称量好的样品和盐酸;将A中盐酸与样品混合;待A中不再有气体产生并恢复至室温后,记录B的液面位置;
(4)用排水法收集H2,排出水的体积等于H2的体积;根据关系式:Fe~H2,样品中的钨的质量分数的计算式为1-$\frac{56V}{22.4a}$;
(5)读取图2C装置液面数据时,应先调整BC液面相平,再平视读数;若样品中含有不溶于酸,也不与酸反应的物质,把此杂质当做钨,则测得钨的质量分数将偏大.
解答 解:(1)①②属于复分解反应,③是分解反应;④为WO3制取W,化合价反应发生变化,属于氧化还原反应,故答案为:④;
(2)操作①之后,分为滤渣和滤液,故为过滤;钨酸钠和浓盐酸反应生成钨酸(H2WO4)和氯化钠;方程式为Na2WO4+2HCl→H2WO4↓+2NaCl;钨酸(H2WO4)酸性很弱,难溶于水,判断B为钨酸(H2WO4);钨酸(H2WO4)加热分解产生三氧化钨(WO3)和水,判断C为三氧化钨(WO3);H2、CO还原氧化钨生成钨;
故答案为:过滤;Na2WO4+2HCl→H2WO4↓+2NaCl;WO3;H2或CO;
(3)为测定其中金属钨的含量(已知金属钨不溶于盐酸),首先检验检查气密性;然后加入称量好的样品和盐酸;将A中盐酸与样品混合;待A中不再有气体产生并恢复至室温后,记录B的液面位置;
故答案为:②①④③;
(4)用排水法收集H2,测得排出水的体积为VL(标准状况下),则H2的体积也为VL;Fe~H2,Fe的物质的量为$\frac{V}{22.4×3}$mol,样品中的钨的质量分数的计算式为1-$\frac{56V}{22.4a}$=$\frac{22.4a-56V}{22.4a}×100%$;
故答案为:V;$\frac{22.4a-56V}{22.4a}×100%$;
(5)读取图2C装置液面数据时,应先调整BC液面相平,再平视读数;若样品中含有不溶于酸,也不与酸反应的物质,把此杂质当做钨,则测得钨的质量分数将偏大;
故答案为:调整BC液面相平;偏大.
点评 本题主要考查工业制备流程、金属的冶炼和化学计算,题目难度不大,本题注意判断A、B、C三种物质.


科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,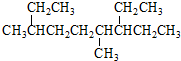 的名称为3,6-二甲基-7-乙基壬烷 的名称为3,6-二甲基-7-乙基壬烷 | |
| B. | 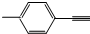 分子中所有原子共平面 分子中所有原子共平面 | |
| C. | 标准状况下,1 L辛烷完全燃烧生成CO28L | |
| D. | 1.0 mol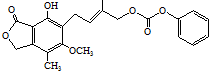 最多能与5.0 mol NaOH水溶液完全反应 最多能与5.0 mol NaOH水溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用催化法处理尾气中的CO和NO:CO+NO$\frac{\underline{\;催化剂\;}}{\;}$C+NO2 | |
| B. | 少量SO2通入到Ba(OH)2溶液:SO2+Ba2++2OH-═BaSO3↓+H2O | |
| C. | NH4HCO3溶于过量的NaOH溶液中:HCO3+OH-═CO32-+H2O | |
| D. | 浓盐酸与二氧化锰供热:Mn2O+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=Q2=Q3=57.3 | B. | Q1>Q2>Q3>57.3 | C. | Q3<Q1<Q2=57.3 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
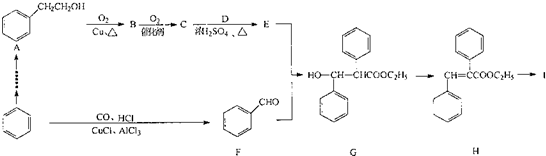
 .
. +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O:E+F--G的反应类型为加成反应.
+2H2O:E+F--G的反应类型为加成反应. +NaOH$\stackrel{△}{→}$C2H5OH+
+NaOH$\stackrel{△}{→}$C2H5OH+ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子的半径:r(A)<r(C)<r(D)<r(E) | |
| B. | 元素B的最简单气态氧化物的稳定性比C的强 | |
| C. | D2C2与A2C2的漂白原理相同 | |
| D. | 元素E的氧化物能溶于B或D的最高价氧化物对应的水化物中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com