
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
���� �ٶ��������ܱ��������������
�ڶ���������HF�ᷴӦ��
�����ӷ�����ˮ�ܷ⣻
��NO������е�������Ӧ��
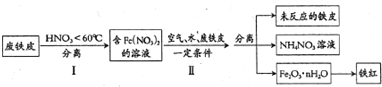
��װ��Fe��NO3��2��Һ���Թ��м���ϡH2SO4������������ԭ��Ӧ����NO��NO�ٱ��������ɶ���������
��� �⣺�ٶ��������ܱ��������������������������ͨ��ʢ������KMnO4��Һ��Ũ�����ϴ��ƿ�õ�����Ķ�����̼������ȷ��
�ڶ���������HF�ᷴӦ���ʴ���
�����ӷ����ڴ��Һ����Լ�ƿ��Ӧ����ˮҺ�⣬����ȷ��
��NO������е�������Ӧ�������ȶ����ڣ��ʴ���
��װ��Fe��NO3��2��Һ���Թ��м���ϡH2SO4������������ԭ��Ӧ����NO��NO�ٱ��������ɶ�������������۲��������ʴ���
��ѡB��
���� ���⿼����������ᴿ��Ϊ��Ƶ���㣬�������ʵ����ʡ����ʲ��켰�������뷽���ǽⱾ��ؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ���ۺ�Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��C��s��ʯī���TC��s�����ʯ����H��0��֪�����ʯ��ʯī�ȶ� | |
| B�� | CO��g��ȼ������283.0��kJ•mol-1����2CO2��g���T2CO��g��+O2��g����H=+566.0kJ•mol-1 | |
| C�� | CH4��g��+2O2��g���TCO2+2H2O��I����H��0���÷�Ӧ�Ļ�ѧ�ܿ���ת��Ϊ���� | |
| D�� | ��֪C��s��+O2��g���TCO2��g����H1��C��s��+$\frac{1}{2}$O2��g���TCO��g����H2����H1����H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
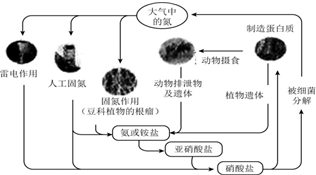
| A�� | ������ѭ���е�Ԫ�ؾ������� | |
| B�� | ��������ʱ�漰��һ����ӦΪN2+2O2�T2NO2 | |
| C�� | ��������ͺ����л�����ת�� | |
| D�� | ��Ȼ�絪ѭ���е�Ԫ�ص����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1��mol•L-1��NaOH��Һ�У�K+��Na+��SO42-��CO32- | |
| B�� | 0.1��mol•L-1��Na2CO3��Һ�У�K+��Ba2+��NO3-��Cl- | |
| C�� | 0.1��mol•L-1��FeCl3��Һ�У�K+NH4+��I-��SCN- | |
| D�� | 0.1��mol•L-1�������У�Fe2+��Na+��Br-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ����Һ�ȡ��ɱ����⻯����Ϊ������ | |
| B�� | ������С�մ��ᡢ�������Ϊ����� | |
| C�� | ��ơ�ţ�̡�������Ư�۾�Ϊ���� | |
| D�� | Na2O2��Na2CO3��Na2SiO3��KNO3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �������Һ�ĵ絼��Խ��������Խǿ����0.100mol•L-1��NaOH��Һ�ζ�10.00mLŨ�Ⱦ�Ϊ0.100mol•L-1 �������CH3COOH��Һ�����ô�������õζ���������Һ�ĵ絼����ͼ��ʾ������˵����ȷ���ǣ�������
�������Һ�ĵ絼��Խ��������Խǿ����0.100mol•L-1��NaOH��Һ�ζ�10.00mLŨ�Ⱦ�Ϊ0.100mol•L-1 �������CH3COOH��Һ�����ô�������õζ���������Һ�ĵ絼����ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ���ߢٴ����ζ�HCl��Һ������ | |
| B�� | A����Һ�У�c��CH3COO-��+c��OH-��-c��H+��=0.1mol•L-1 | |
| C�� | ����ͬ�¶��£�A��B��C������Һ��ˮ�ĵ���̶ȣ�C��B��A | |
| D�� | D����Һ�У�c��Cl-��=2c��OH-��-2c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
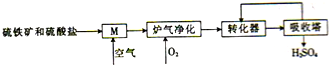 ú����Ҫ�Ļ���ԭ�ϣ�ú������ɼ��ٻ�������Ⱦ������ú��ʯ�е���������Ҫ�ɷ�ΪFeS2�����̵�����õ�����������������Ĺ���������ͼ��ʾ��
ú����Ҫ�Ļ���ԭ�ϣ�ú������ɼ��ٻ�������Ⱦ������ú��ʯ�е���������Ҫ�ɷ�ΪFeS2�����̵�����õ�����������������Ĺ���������ͼ��ʾ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com