
铜粉放入稀硫酸溶液中,加热后无明显现象发生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出。该盐是( )
A.Fe2(SO4)3 B.Na2CO3 C.KNO3 D.FeSO4
科目:高中化学 来源: 题型:
用含有A12O3、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
H2SO4溶解A12O3的离子方程式是
KMnO4 - 氧化Fe2+的离子方程式补充完整:
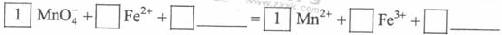
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1mol·L-1
根据表中数据解释步骤Ⅱ的目的: 。
(4)己知:一定条件下,MnO4 - 可与Mn2+反应生成MnO2。
① 向 Ⅲ 的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是 。
② Ⅳ 中加入MnSO4的目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同
B.制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸
C.用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率
D.用AgNO3溶液可以鉴别KCl和KI
查看答案和解析>>
科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5。
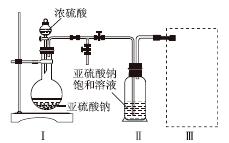
(1)装置Ⅰ中产生气体的化学方程式为______________________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是______。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
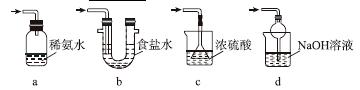
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO 的电离程度大于水解程度,可采用的实验方法是________(填序号)。
的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检测Na2S2O5晶体在空气中已被氧化的实验方案是
________________________________________________________________________
________________________________________________________________________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O===H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于浓H2SO4.稀H2SO4的叙述中正确的是( )
A. 浓H2SO4.稀H2SO4都难挥发
B. 浓H2SO4.稀H2SO4都能氧化金属Zn,且反应实质相同
C. 浓H2SO4.稀H2SO4在加热时都能与铜反应
D.浓H2SO4.稀H2SO4在常温下都能用铁制容器贮存
查看答案和解析>>
科目:高中化学 来源: 题型:
铁和铜的混合物中加入不足量的硝酸,反应后剩余金属m1g;再向其中加入一定量该硝酸,充分振荡后,剩余金属m2 g,则m1.m2之间的关系正确的是 ( )
A.m1一定大于m2 B.m1可能等于m2 C.m1一定等于m2 D.m1不可能大于m2
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列化学方程式
(1)Cu与浓硫酸反应 _____________________________________________________
(2)C与浓硫酸反应 ______________________________________________________
(3)Cu与浓硝酸反应 _____________________________________________________
(4)Cu与稀硝酸反应 _____________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
我国缺碘病区甚广,防治缺碘病的主要措施是食盐中加碘.1996年我国政府以国家标准的方式规定食盐的碘添加剂是KIO3.
(1)可用盐酸酸化的KI淀粉混合物检验食盐是否为加碘盐,反应的化学方程式为 .
(2)可用电化学方法制备KIO3.原理是:以石墨为阳极,不锈钢为阴极,以KI溶液(加入少量K2Cr2O7)为电解质溶液,在一定电流强度和温度下进行电解,其电解总反应方程式为KI+3H2O KIO3+3H2↑.试写出两极反应式:阳极 ;阴极 .
KIO3+3H2↑.试写出两极反应式:阳极 ;阴极 .
(3)如果在容积为10L的离子交换膜电解槽中,1min时阴极可产生11.2L(标准状况)Cl2,这时溶液的pH是(设体积维持不变) .
(4)Cl2常用于自来水的消毒杀菌,现有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl﹣,消毒等量的自来水,所需Cl2和ClO2的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式书写正确的是( )
|
| A. | 2SO2+O2=2SO3 △H=﹣196.6kJ•mol﹣1 |
|
| B. | H2(g)+ |
|
| C. | 2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJ |
|
| D. | C(s)+O2(g)=CO2(g)△H=+393.5kJ•mol﹣1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com