
分析 锌片、银片、稀硫酸构成原电池,活泼金属锌作负极,负极上失电子发生氧化反应,银作正极,正极上得电子发生还原反应,电解质中的阳离子移向正极,依据该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,分析判断电极质量减小为反应的锌的质量为13g,依据电极反应和电子守恒计算生成的气体物质的量得到气体体积.
解答 解:锌片、银片、稀硫酸构成原电池,活泼金属锌作负极,负极上失电子发生氧化反应,银作正极,正极上得电子发生还原反应,电解质中的阳离子移向正极;若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,分析可知电极质量减小的是负极反应的锌的质量,物质的量=$\frac{60g-47g}{65g/mol}$=0.2mol;锌做负极,失电子发生氧化反应,电极反应为:Zn-2e-═Zn2+,银片做正极,溶液中氢离子在银电极得到电子发生还原反应,电极反应为:2H++2e-═H2↑,依据电子守恒可知,转移电子物质的量为0.4mol,生成氢气物质的量为0.2mol,标准状况下体积=0.2mol×22.4L/mol=4.48L,
故答案为:氧化;正极;4.48 L.
点评 本题考查了原电池原理的分析判断,电极反应,电极名称,电子守恒的计算应用,掌握基础是解题关键,题目较简单


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 3-甲基-2-乙基戊烷 | |
| B. | (CH3)3CCH2CH(C2H5)CH3 2,2-二甲基-4-乙基戊烷 | |
| C. | 2-甲基-3-戊炔 | |
| D. | 邻甲基苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 火力发电在我国的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题,直接排放含SO2的烟气会形成酸雨,危害环境.
火力发电在我国的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题,直接排放含SO2的烟气会形成酸雨,危害环境.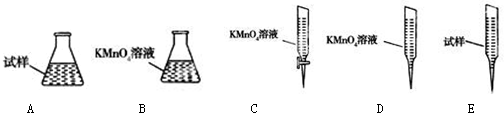
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1000ωνρ}{36.5}$mol/L | B. | $\frac{1000νρ}{36.5+22400}$mol/L | ||
| C. | $\frac{ων}{22.4(V+1)}$mol/L | D. | $\frac{1000νρ}{36.5V+22400}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 氢化物的沸点R>X | |
| B. | 原子半径:W>R>X | |
| C. | 气态氢化物的稳定性:X>Y | |
| D. | X、Z形成的化合物中可能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
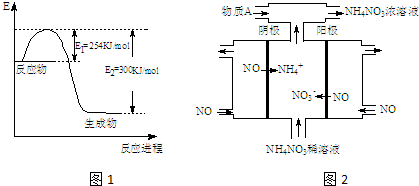
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
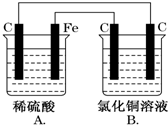 烧杯A中盛放0.1mol•L-1的H2SO4溶液,烧杯B中盛放0.1mol•L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )
烧杯A中盛放0.1mol•L-1的H2SO4溶液,烧杯B中盛放0.1mol•L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )| A. | A为原电池,B为电解池 | |
| B. | A中阳离子向碳极移动,阴离子向铁极移动 | |
| C. | 当A烧杯中产生0.1 mol气体时,B烧杯中产生气体的物质的量也为0.1 mol | |
| D. | 一段时间后,B烧杯中溶液的浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | H2SO4 | 冰醋酸 | 水银 |
| B | 冰醋酸 | 福尔马林 | 苛性钠 | 碘化氢 | 乙醇 |
| C | 火碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
| D | 胆矾 | 氯水 | 硫酸钡 | 次氯酸 | 氨气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com