
| A.SO2和SiO2 | B.CO2和H2O | C.Na2O2和H2O2 | D.NaCl和HCl |
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案科目:高中化学 来源:不详 题型:填空题
| 微粒 | a | b | c | d | e | f | g |
| 原子核数 | 双核 | 双核 | 三核 | 四核 | 四核 | 五核 | 五核 |
| 所带单位电荷 | 0 | -1 | 0 | 0 | +1 | | +1 |
 ④Ni2+可与d形成配位数为6的配离子,该配离子的化学式为 。
④Ni2+可与d形成配位数为6的配离子,该配离子的化学式为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.碳酸氢根离子的电离方程式: HCO3-+H2O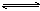 H3O++ CO32- H3O++ CO32- |
| B.从上到下,卤族元素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱 |
| C.因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S |
| D.NaCl晶体中每个Na+同时吸引着6个Cl-,CsCl晶体中每个Cl-同时吸引着6个Cs+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在氯化钠晶体中,只有阴离子和阳离子,没有NaCl分子 |
| B.在氯化钠晶体中存在NaCl分子 |
| C.石英是由SiO2形成的分子晶体 |
| D.金刚石和石墨晶体都是由碳原子网状结构形成的典型的原子晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.全部由非金属元素组成的化合物一定不是离子化合物 |
| B.金属原子与非金属原子之间的化学键可能是离子键,也可能是共价键 |
| C.晶体中有阳离子,则必定有阴离子 |
| D.晶体中有阴离子,则必定有阳离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.存在四面体结构单元,O处于中心,Si处于4个顶角 |
| B.最小的环上,有3个Si原子和3个O原子 |
| C.最小的环上,Si和O原子数之比为1:2 |
| D.最小的环上,有6个Si原子和6个O原子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔沸点:单晶硅>碳化硅>金刚石 | B.熔沸点:MgO>NaCl>KCl |
| C.熔沸点:Na>Mg>Al | D.熔沸点:O2>I2>Hg |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| | 表述1 | 表述2 | ||
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |