
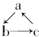 (“→”表示一步完成)关系相互转化的有( )
(“→”表示一步完成)关系相互转化的有( )| 物质 编号 | a | b | c |
| 1 | Al2O3 | NaAlO2 | Al(OH)3 |
| 2 | FeO | Fe(NO3)2 | Fe(OH)2 |
| 3 | MgCl2 | Mg(OH)2 | MgO |
| 4 | CuO | CuSO4 | Cu(OH)2 |
| 5 | Si | SiO2 | H2SiO3 |
| 6 | C | CO | CO2 |
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
分析 1.氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠与弱酸反应生成氢氧化铝,氢氧化铝分解生成氧化铝;
2.氧化亚铁与硝酸反应生成硝酸铁;
3.氯化镁与氢氧化钠反应生成氢氧化镁,氢氧化镁分解生成氧化镁,氧化镁与盐酸反应生成氯化镁;
4.氧化铜与硫酸反应生成硫酸铜,硫酸铜与氢氧化钠反应生成氢氧化铜,氢氧化铜分解生成氧化铜;
5.二氧化硅与水不反应;
6.碳和少量氧气反应生成一氧化碳,一氧化碳与氧气反应生成二氧化碳,二氧化碳与镁反应生成碳.
解答 解:1.反应关系为Al2O3$\stackrel{NaOH}{→}$NaAlO2$\stackrel{NaOH}{→}$Al(OH)3$\stackrel{加热}{→}$Al2O3,可实现,故正确;
2.氧化亚铁与硝酸反应生成硝酸铁,故错误;
3.反应关系为MgCl2$\stackrel{NaOH}{→}$Mg(OH)2$\stackrel{加热}{→}$MgO$\stackrel{HCl}{→}$MgCl2,可实现,故正确;
4.反应关系为CuO$\stackrel{硫酸}{→}$CuSO4$\stackrel{NaOH}{→}$Cu(OH)2$\stackrel{加热}{→}$CuO,可实现,故正确;
5.二氧化硅与水不反应,故错误;
6.反应关系为C$\stackrel{氧气}{→}$CO$\stackrel{氧气}{→}$CO2$\stackrel{Mg}{→}$C,可实现,故正确;
故选B.
点评 本题考查了物质之间通过一步反应的原理,为高频考点,根据常见化学物质的性质,通过列举具体反应,判断物质间是否可以实现一步反应的转化,采用排除法(即发现一步转化不能实现,排除该选项)是解答本题的捷径,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 0.2mol•L-1 Na2SO4溶液中含有Na+和SO42-总物质的量为0.6mol | |
| B. | 50mL 2mol•L-1的NaCl溶液和100 mL L 0.5mol•L-1MgCl2溶液中,Cl-的物质的量浓度相等 | |
| C. | 用1L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1mol•L-1 | |
| D. | 10g 98%的硫酸(密度为1.84g•cm-3)与10mL 18.4mol•L-1的硫酸的浓度是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 现象或反应 | 原理解释 |
| A | 2CO=2C+O2在任何条件下均不能自发进行 | 该反应△H>0,△S>0 |
| B | 铝箔在酒精灯火焰上加热融化但不滴落 | Al2O3熔点高于Al单质 |
| C | 蒸馏时,温度计的球泡应靠近蒸馏烧瓶支管口处 | 此位置指示的是被蒸馏物质的沸点 |
| D | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
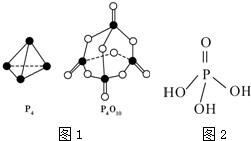
| 化学键 | P-P | P-O | P═O | O═O |
| 键能/kJ•mol-1 | a | b | c | d |
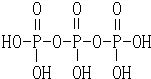 ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
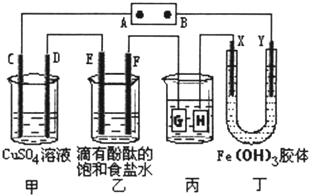 如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深.请回答:
如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | 在NaClO溶液中通入过量SO2气体:ClO-+H2O+SO2═HClO+HSO3- | |
| C. | NaHCO3与少量Ca(OH)2溶液反应:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 10mL 0.5mol/L的明矾溶液与20mL 0.5mol/L的Ba(OH)2溶液混合反应:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ②③④ | C. | ①③⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应在较高温度下才能自发进行 | |
| B. | 该反应的正反应活化能小于逆反应活化能 | |
| C. | 该反应中,断裂化学键的总键能大于形成化学键的总键能 | |
| D. | 若NH3和O2的混合气发生上述反应,气体通入足量水中,剩余气体一定是O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com