
����Ŀ��������������ȼ������ˮ���Ȼ�ѧ����ʽ��H2��g��+1/2O2��g���TH2O��g����H=akJ/mol
2H2��g��+O2��g���T2H2O��l����H=bkJ/mol
��ش��������⣺����ʾ��|b|��ʾb�ľ���ֵ��
��1����2molH2��ȫȼ������ˮ��������ų�������|b|kJ�����������������=����
��2����Ӧ�ȵĹ�ϵ��2ab�����������������=������
��3������֪H2��g��+1/2O2��g���TH2O��g����H=��242kJ/mol����������1mol O=O����ȫ����ʱ��������496kJ��ˮ������1mol H��O���γ�ʱ�ų�����463kJ����������1molH��H������ʱ���յ�����Ϊ ��
���𰸡�
��1����
��2����
��3��436 kJ
���������⣺��1��Һ̬ˮ������̬ˮʱҪ���ȣ���2H2��g��+O2��g���T2H2O��l����H=bkJ/mol��֪����2molH2��ȫȼ������ˮ��������ų�������С��|b|kJ�����Դ��ǣ�������2����֪����H2��g��+1/2O2��g���TH2O��g����H=akJ/mol����2H2��g��+O2��g���T2H2��l����H=bkJ/mol�����ø�˹���ɣ����١�2���٣�
�ɵã�2H2O��l���T2H2O��g������H=��2a��b��kJ/mol��
��Һ̬ˮ������̬ˮʱҪ���ȣ���
2a��b��0��
���ԣ�2a��b��
���Դ��ǣ�������3����֪H2��g��+1/2O2��g���TH2O��g����H=��242kJ/mol����H��H������ʱ���յ�����ΪxkJ��
���ݷ�Ӧ�ȵ��ڷ�Ӧ����ܼ��ܼ�ȥ��������ܼ��ܣ���
x+ ![]() ��496��2��463=��242��
��496��2��463=��242��
��x=436��
���Դ��ǣ�436��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣�����բ������ڱ��е�λ�ã��û�ѧ����ش��������⣺

��1��Ԫ�آ��γɵĵ��ʵĵ���ʽΪ_________��Ԫ�آ��γɵ����������ĽṹʽΪ________��
��2����������������Ԫ���γɵ��⻯���У����ȶ�����ǿ����_________���ѧʽ�����е���ߵ���__________���ѧʽ����
��3��Ԫ�آ������ڱ��е�λ��_________����Ԫ�صĵ�����Ҫ��;________����һ�֣���
��4��������Ԫ�ص�����������ˮ��������ǿ���Ƚ�__________(�ѧʽ����
��5����������Ԫ�ص�����������ˮ����֮�䷴Ӧ�����ӷ���ʽΪ___________��
��6���õ���ʽ��ʾ��������Ԫ�ؽ�ϳɻ�������γɹ���__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NH3�������л��ܼ����Ȼ�̼������װ�ò�������NH3β�����յ��ǣ� ��
A.
B.
C.
D.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һЩ���� ![]() C��
C�� ![]() K��
K�� ![]() Ca��
Ca�� ![]() C��
C�� ![]() N��
N�� ![]() Ar����
Ar����
��1����Ϊͬλ�ص�������
��2����������ȣ������ܻ���ͬλ�ص�������
��3����������ȣ�������������ȵ��������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊԭ����ȡ�Ҷ���(HOOC��COOH)�Ĺ����У�Ҫ���ξ������в����е�(����)
����NaOH��ˮ��Һ���ȡ�����NaOH�Ĵ���Һ���� ����Ũ���Ṳ�ȵ�170�桡���ڴ��������������������Ӧ������Cu��Ag���ڵ���������������ȡ��������Ƶ�Cu(OH)2����Һ����
A.�٢ۢܢڢ�
B.�٢ۢܢڢ�
C.�ڢܢ٢ݢ�
D.�ڢܢ٢ޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���ǣ� ��
A.����ϡ���2Fe+6H+�T2Fe3++3H2��
B.̼�������ϡ���HCO ![]() +H+�TH2O+CO2��
+H+�TH2O+CO2��
C.�����Ȼ�ͭ��Һ��Ӧ��Al+Cu2+�TAl3++Cu
D.�����������O2��+2H+�TH2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯������ͨ��һ��ʵ��ֱ����ɵ���
A. Al(OH)3��Al2O3 B. Al��AlO2-
C. Al2O3��Al(OH)3 D. Al3+��Al(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������������˫��Ĥ���ҵ��۴�����ˮ�е�NH4+,ģ��װ����ͼ��ʾ������˵����ȷ���ǣ� ��
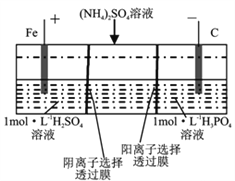
A. ��������Һ����ɫ����ػ�ɫ
B. �����ĵ缫��ӦʽΪ��4OH--4e-=2H2O+O2��
C. ���һ��ʱ�����������Һ�е�pH����
D. ���һ��ʱ�����������Һ�е�����һ����(NH4)3PO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������е�һ�ֳ�����������;�dz��㷺��
��1��FeCl3��Һ���ڸ�ʴӡˢ��·�壬��Ӧ�����ӷ���ʽΪ
��2���÷���Ƥ��ȡ����۵ľֲ�����ͼ���£�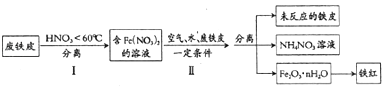
�ٲ���I�¶Ȳ���̫�ߵ�ԭ����
�ڲ�����з�����Ӧ��
4Fe��NO3��2+O2+��2n+4��H2O�T24Fe2O3H2O+8HNO3
4Fe+10HNO3�T4Fe��NO3��2+NH4NO3+3H2O
��һ����Ӧ����������
�ʶ�����Ӧÿ����1molNH4NO3 �� ת�Ƶĵ�������
����������ں��Ӹֹ죬�䷴Ӧ�Ļ�ѧ����ʽΪ
���������������������е�Ԫ������Ҫ�Ĵ�����ʽΪ������ĸ��
a���������� b�����ᰴ c���������� d�����ᣮ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com