
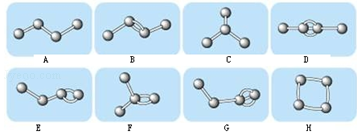
分析 小球表示碳原子,小棍表示化学键,每个C形成4个键,由球棍模型可知A为丁烷,B为2-丁烯,C为2-甲基丙烷,D为2-丁炔,E为1-丁烯,F为2-甲基丙烯,G为1-丁炔,H为环丁烷,以此解答.
解答 解:(1)分子式相同,结构不同的有机物互为同分异构体,A为丁烷,A与C、B为2-丁烯,B与EFH、D为2-丁炔,D与G的分子式相同,结构不同,互为同分异构体,
故答案为:C;EFH; G;
(2)碳原子之间成键方式具有多样性,碳原子与碳原子之间不仅可以形成共价单键,还可以形成双键、单键,不仅可以形成碳链还可以形成碳环,
故答案为:碳碳双键;碳碳叁键; 碳链;
(3)按照碳碳间成键方式烃可分为烷烃、烯烃、炔烃,烷烃分子中,碳原子和其他原子均以单键成键,烷烃只含单键,成链状,烯烃含有碳碳双键,炔烃含有碳碳三键,根据图示的球棍模型可以看出,BEF属于烯烃,DG属于炔烃,H属于环烷烃,只有A、C中碳原子和其他原子以共价单键结合,属于烷烃,
故答案为:AC.
点评 本题考查有机物的结构、有机化合物中碳的成键特征、同分异构体等知识,题目难度不大,注意掌握对信息的理解运用、读图方法,本题能够加深对同分异构体概念的理解,培养学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:解答题


 .
. .
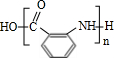
. 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有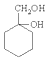 最合理的方案.
最合理的方案.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫原子的原子结构示意图: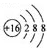 | |
| B. | 原子核内有10个质子的氧原子${\;}_{8}^{18}$O | |
| C. | NH4Cl的电子式: | |
| D. | 邻氯甲苯的结构简式: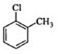 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铁、铜及其化合物在日常生产、生活有着广泛的应用.请回答下列问题:
铁、铜及其化合物在日常生产、生活有着广泛的应用.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3和 NaOH | B. | NaHSO4和Ba(OH)2 | C. | NaAlO2和 H2SO4 | D. | Na2CO3和盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室蒸馏石油时,蒸馏烧瓶中加入一些碎瓷片,为防止暴沸,冷凝管下口进冷水上口出热水 | |
| B. | 实验室制备硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| C. | 实验使手指不小心沾上苯酚,立即用70℃以上的热水清洗 | |
| D. | 检验蔗糖是否水解:蔗糖溶液在稀硫酸存在下水浴加热一点时间后,再与银氨溶液混合加热,观察现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CH4的电极为负极 | B. | 正极发生氧化反应 | ||
| C. | 溶液中的OH-向负极移动 | D. | 工作一段时间后应补充KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡时HI的分解率20% | B. | 反应起始时固体NH4I是5 mol | ||
| C. | 平衡时,c (NH3)=4.5mol/L | D. | 平衡时HI的分解率10% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com