
| A. | 准确量取20.00mL高锰酸钾溶液,可选用25mL碱式滴定管 | |
| B. | 将水加热,Kw增大,pH不变 | |
| C. | 用惰性电极电解1L浓度均为2mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 mol 电子转移时,阴极析出6.4g金属 | |
| D. | NaAlO2的水溶液经加热浓缩、蒸干灼烧后能得到NaAlO2固体 |
分析 A.高锰酸钾可氧化橡胶;
B.水的电离为吸热反应;
C.用惰性电极电解1L浓度均为2mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 mol 电子转移时,只有银离子得到电子;
D.NaAlO2的水溶液,水解产物不挥发.
解答 解:A.高锰酸钾可氧化橡胶,则准确量取20.00mL高锰酸钾溶液,可选用25mL酸式滴定管,故A错误;
B.水的电离为吸热反应,则将水加热,Kw增大,氢离子浓度增大,pH减小,故B错误;
C.用惰性电极电解1L浓度均为2mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 mol 电子转移时,只有银离子得到电子,阴极析出Ag的质量为0.2mol×108g/mol=21.6g,故C错误;
D.NaAlO2的水溶液,水解产物不挥发,则经加热浓缩、蒸干灼烧后能得到NaAlO2固体,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握仪器的使用、电解、电离、水解为解答的关键,侧重分析与实验能力的考查,注意反应原理与实验的结合,题目难度不大.


科目:高中化学 来源: 题型:选择题
 现代建筑的门窗架常用电解加工成的古铜色硬铝制造.取硬铝样品进行如下实验(每一步试剂均过量),由此可以推知硬铝的组成可能为( )
现代建筑的门窗架常用电解加工成的古铜色硬铝制造.取硬铝样品进行如下实验(每一步试剂均过量),由此可以推知硬铝的组成可能为( )| A. | Al、Mg、SiO2、Zn | B. | Al、Fe、Zn、Na | C. | Al、Na、Cu、Fe | D. | Al、Cu、Mg、Si |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
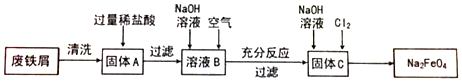
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 步骤①、③的操作都是过滤 | |
| B. | 可用淀粉溶液检验步骤②的反应是否进行完全 | |
| C. | 步骤③中加入的有机溶剂是乙醇 | |
| D. | 步骤④的操作是精馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
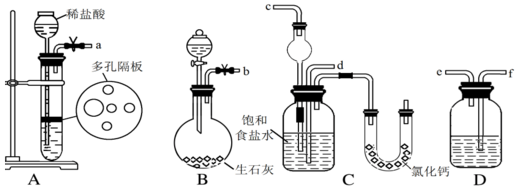
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 min内,Y的平均反应速率为0.03 mol•L-1•s-1 | |
| B. | 10 min内,X和Y反应放出的热量为a kJ | |
| C. | 10 min内,消耗0.2 mol X,生成0.4 mol Z | |
| D. | 10 min内,前5minX的平均反应速率与后5minX的平均反应速率相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=b | |
| B. | 混合溶液的pH=7 | |
| C. | 混合溶液中c(H+)=$\sqrt{Kw}$ mol?L-1 | |
| D. | 向反应后的混合液中滴加石蕊试液后呈紫色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com