
·ÖĪö £Ø1£©0.2mol•L-1µÄ£ØNH4£©Al£ØSO4£©2ČÜŅŗÖŠļ§øłŗĶĀĮĄė×ÓĖ®½ā£¬°±Ė®¼īŠŌ“óÓŚĒāŃõ»ÆĀĮ£¬ŌņĀĮĄė×ÓĖ®½ā³Ģ¶Č“óÓŚļ§øł£¬c£ØAl3+£©£¼c£ØNH4+£©£»
£Ø2£©ŌŚNaHCO3ČÜŅŗÖŠ“ęŌŚĢ¼ĖįĒāøłĄė×ÓµÄĖ®½āĘ½ŗā”¢µēĄėĘ½ŗāŗĶĖ®µÄµēĄėĘ½ŗā£»
£Ø3£©ŃĒĢśĄė×ÓŗĶļ§øłĖ®½ā¾łĻŌĖįŠŌ£¬ŃĒĢśĄė×ÓĖ®½āŅÖÖĘļ§øłµÄĖ®½ā£¬£ØNH4£©2Fe£ØSO4£©2ČÜŅŗÖŠc£ØNH4+£©ÉŌ“ó£¬ŅŌ“Ė½ā“šøĆĢā£»
£Ø4£©Ģ¼ĖįÄĘČÜŅŗÓėČżĀČ»ÆĢśČÜŅŗ·¢ÉśĖ«Ė®½āÉś³ÉĒāŃõ»ÆĢśŗĶ¶žŃõ»ÆĢ¼ŗĶĖ®£»
£Ø5£©Fe£ØNO3£©3ŹĒĒæĖįČõ¼īŃĪ£¬¼ÓČČ¹ż³ĢÖŠ·¢ÉśĖ®½āÉś³ÉFe£ØOH£©3ŗĶHNO3£¬HNO3¾ßÓŠ»Ó·¢ŠŌ£¬¼ÓČČ“Ł½ųHNO3»Ó·¢£¬“Ó¶ų“Ł½ųĀČ»ÆĢśĖ®½ā£¬ÕōøÉŹ±µĆµ½¹ĢĢåFe£ØOH£©3£¬×ĘÉÕFe£ØOH£©3µĆµ½Fe2O3£»
£Ø6£©ÓĆSOCl2ÓėAlCl3•6H2O»ģŗĻ¹²ČČ£¬æɵĆĪŽĖ®AlCl3£¬ŹĒŅņSOCl2ÓėĖ®·“Ó¦¼Č¼õÉŁĖ®µÄĮæ£¬Éś³ÉµÄHClÓÖŅÖÖĘĮĖAlCl3µÄĖ®½ā£»
£Ø7£©¼ÓČėµÄŃõ»Æ¼ĮÄܹ»½«ŃĒĢśĄė×ÓŃõ»ÆĪļĢśĄė×Ó£¬²¢ĒŅ²»ÄÜ“ųČėŌÓÖŹ£»
µ÷½ŚČÜŅŗpHµÄ¹ż³ĢÖŠ£¬¼ÓČėµÄĪļÖŹ¼“Äܹ»ÓėĒāĄė×Ó·“Ó¦£¬ÓÖ²»“ųČėŌÓÖŹ£¬Ōņ¼Óŗ¬ĶŌŖĖŲµÄĪļÖŹÓėĒāĄė×Ó·“Ó¦“Ł½ųĢśĄė×ÓĖ®½ā×Ŗ»ÆĪŖ³Įµķ£®
½ā“š ½ā£ŗ£Ø1£©0.2mol•L-1µÄ£ØNH4£©Al£ØSO4£©2ČÜŅŗÖŠļ§øłŗĶĀĮĄė×ÓĖ®½ā£¬°±Ė®¼īŠŌ“óÓŚĒāŃõ»ÆĀĮ£¬ŌņĀĮĄė×ÓĖ®½ā³Ģ¶Č“óÓŚļ§øł£¬c£ØAl3+£©£¼c£ØNH4+£©£¬ČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ£ŗc£ØSO42-£©£¾c£ØNH4+£©£¾c£ØAl3+£©£¾c£ØH+£©£¾c£ØOH-£©£¬
¹Ź“š°øĪŖ£ŗc£ØSO42-£©£¾c£ØNH4+£©£¾c£ØAl3+£©£¾c£ØH+£©£¾c£ØOH-£©£»
£Ø2£©ŌŚNaHCO3ČÜŅŗ“ęŌŚĢ¼ĖįĒāøłĄė×ÓµÄĖ®½āĘ½ŗāĪŖ£ŗHCO3-+H2O?H2CO3+OH-£¬µēĄėĘ½ŗā£ŗHCO3-?H++CO32-£¬Ė®µÄµēĄėĘ½ŗāH2O?H++OH-£¬
¹Ź“š°øĪŖ£ŗHCO3-+H2O?H2CO3+OH-£»HCO3-?H++CO32-£¬H2O?H++OH-£»
£Ø3£©£ØNH4£©2Fe£ØSO4£©2ÖŠNH4+ŗĶFe2+¶¼Ė®½ā³ŹĖįŠŌ£¬Ė®½āĻą»„ŅÖÖĘ£¬Ņņ“Ė£ØNH4£©2Fe£ØSO4£©2ÖŠNH4+µÄĖ®½ā³Ģ¶Č£ØNH4£©2SO4µÄŅŖŠ”£¬£ØNH4£©2Fe£ØSO4£©2±Č£ØNH4£©2SO4µÄc£ØNH4+£©“ó£®
¹Ź“š°øĪŖ£ŗ£ØNH4£©2Fe£ØSO4£©2£»NH4+ŗĶFe2+¶¼Ė®½ā³ŹĖįŠŌ£¬Ė®½āĻą»„ŅÖÖĘ£»
£Ø4£©Ģ¼ĖįÄĘČÜŅŗÓėČżĀČ»ÆĢśČÜŅŗ·¢ÉśĖ«Ė®½ā£¬Ąė×Ó·½³ĢŹ½ĪŖ?2Fe3++3CO32-+3H2O=2Fe£ØOH£©3”ż+3CO2 ??”ü£¬
¹Ź“š°øĪŖ£ŗ?2Fe3++3CO32-+3H2O=2Fe£ØOH£©3”ż+3CO2 ??”ü£»
£Ø5£©Fe£ØNO3£©3ŹĒĒæĖįČõ¼īŃĪ£¬¼ÓČČ¹ż³ĢÖŠ·¢ÉśĖ®½āÉś³ÉFe£ØOH£©3ŗĶHNO3£¬·“Ó¦·½³ĢŹ½ĪŖFe£ØNO3£©3+3H2O?Fe£ØOH£©3+3HNO3£¬HNO3¾ßÓŠ»Ó·¢ŠŌ£¬¼ÓČČ“Ł½ųHNO3»Ó·¢£¬“Ó¶ų“Ł½ųĀČ»ÆĢśĖ®½ā£¬ÕōøÉŹ±µĆµ½¹ĢĢåFe£ØOH£©3£¬×ĘÉÕFe£ØOH£©3µĆµ½Fe2O3£¬·“Ó¦·½³ĢŹ½ĪŖ2Fe£ØOH£©3$\frac{\underline{\;\;”÷\;\;}}{\;}$Fe2O3+3H2O£¬ĖłŅŌ×īÖÕµĆµ½µÄ¹ĢĢåŹĒFe2O3£¬
¹Ź“š°øĪŖ£ŗFe2O3£»ĻõĖįĢśĖ®½āÉś³ÉFe£ØOH£©3ŗĶHNO3£¬·“Ó¦·½³ĢŹ½ĪŖFe£ØNO3£©3+3H2O?Fe£ØOH£©3+3HNO3£¬HNO3¾ßÓŠ»Ó·¢ŠŌ£¬¼ÓČČ“Ł½ųHNO3»Ó·¢£¬“Ó¶ų“Ł½ųĀČ»ÆĢśĖ®½ā£¬ÕōøÉŹ±µĆµ½¹ĢĢåFe£ØOH£©3£¬×ĘÉÕFe£ØOH£©3µĆµ½Fe2O3£»
£Ø6£©SOCl2ÓėĖ®·“Ӧɜ³ÉµÄĀČ»ÆĒā»į¶ŌĀČ»ÆĀĮĖ®½āĘšµ½ŅÖÖĘ×÷ÓĆ£»·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗSOCl2+H2O=2HCl”ü+SO2”ü£¬ÕōøÉAlCl3ČÜŅŗ²»ÄܵƵ½ĪŽĖ®AlCl3£¬Ź¹SOCl2ÓėAlCl3•6H20»ģŗĻ²¢¼ÓČČ£¬æɵƵ½ĪŽĖ®AlCl3£¬SOCl2ÓėĖ®·“Ӧɜ³ÉµÄĀČ»ÆĒā»į¶ŌĀČ»ÆĀĮĖ®½āĘšµ½ŅÖÖĘ×÷ÓĆ£¬
¹Ź“š°øĪŖ£ŗSOCl2ÓėĖ®·“Ó¦¼ČæɼõÉŁĖ®µÄĮæ£¬Éś³ÉµÄHClÓÖŅÖÖĘĮĖAlCl3µÄĖ®½ā£»
£Ø7£©Óū³żČ„ĖįŠŌĮņĖįĶČÜŅŗÖŠµÄÉŁĮæĮņĖįŃĒĢśŌÓÖŹ£¬ŌŚĢį“æŹ±ĪŖĮĖ³żČ„Fe2+£¬³£¼ÓČėŗĻŹŹŃõ»Æ¼Į£¬æÉŅŌŹĒH2O2£¬Ę仹Ō²śĪļŹĒĖ®£¬ĪŽŌÓÖŹ£¬
A£®KMnO4»įÉś³ÉĆĢĄė×Ó£¬¹ŹA“ķĪó£»
B£®Cl2 ŗĶĖ®·“Ó¦Ė®»įÉś³ÉĀČĄė×Ó£¬¹ŹB“ķĪó£»
C£®30%¹żŃõ»ÆĒāČÜŅŗ£¬²»»įŅżČėŠĀµÄŌÓÖŹ£¬ĒŅÄÜŃõ»ÆŃĒĢśĄė×Ó£¬¹ŹCÕżČ·£»
D£®Ļ”ĮņĖį²»ÄÜŃõ»ÆŃĒĢśĄė×Ó£¬¹ŹD“ķĪó£»
E£®ÅØĮņĖįČÜÓŚĖ®·ÅČČ“Ł½ųĖ®½ā£¬²»Ņ×æŲÖĘ£¬¹ŹE“ķĪó£»
¼ÓČėŹŹµ±ĪļÖŹµ÷ÕūÖĮČÜŅŗpH=4£¬Ź¹Fe3+×Ŗ»ÆĪŖFe£ØOH£©3£¬ĪŖ±ÜĆā“ųČėŌÓÖŹ£¬æÉŃ”ÓĆCuO”¢Cu£ØOH£©2£¬CuCO3µČ£¬
¹Ź“š°øĪŖ£ŗC£»CuO”¢Cu£ØOH£©2£¬CuCO3£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃĪĄąĖ®½āµÄÓ¦ÓĆ£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”µÄ±Č½Ļ£¬ČÜŅŗÖŠĘ½ŗāµÄ·ÖĪö£¬ČÜŅŗÅäÖʵČÖŖŹ¶£¬×¢ŅāÖŖŹ¶µÄ¹éÄÉŗĶÕūĄķŹĒ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
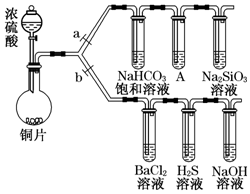 øł¾ŻŅŖĒóĶź³ÉĻĀĮŠŹµŃé¹ż³Ģ£Øa”¢bĪŖµÆ»É¼Š£¬¼ÓČČ¼°¹Ģ¶Ø×°ÖĆŅŃĀŌČ„£©£®
øł¾ŻŅŖĒóĶź³ÉĻĀĮŠŹµŃé¹ż³Ģ£Øa”¢bĪŖµÆ»É¼Š£¬¼ÓČČ¼°¹Ģ¶Ø×°ÖĆŅŃĀŌČ„£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ¼× | ŅŅ |  | |
| A | NH4NO3”¢Al£ØNO3£©3”¢HCl”¢Fe£ØNO3£©3 | NaOH | |
| B | Na2CO3”¢NH4HCO3”¢Na2SO4 | Ba£ØOH£©2 | |
| C | AlCl3”¢Mg£ØNO3£©2”¢HNO3 | NaOH | |
| D | NaAlO2”¢NH3•H2O”¢NaOH | H2SO4 |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
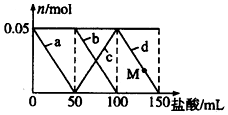 Ļņŗ¬Na2CO3”¢NaAlO2µÄ»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČė150mL 1mol•L-1µÄHClČÜŅŗ£¬²āµĆČÜŅŗÖŠµÄij¼øÖÖĄė×ÓĪļÖŹµÄĮæµÄ±ä»ÆČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
Ļņŗ¬Na2CO3”¢NaAlO2µÄ»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČė150mL 1mol•L-1µÄHClČÜŅŗ£¬²āµĆČÜŅŗÖŠµÄij¼øÖÖĄė×ÓĪļÖŹµÄĮæµÄ±ä»ÆČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | aĒśĻß±ķŹ¾µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗAlO2-+H++H2O=Al£ØOH£©3 | |
| B£® | bŗĶcĒśĻß±ķŹ¾µÄĄė×Ó·“Ó¦ŹĒĻąĶ¬µÄ | |
| C£® | MµćŹ±Al£ØOH£©3µÄÖŹĮæŠ”ÓŚ3.9g | |
| D£® | Ō»ģŗĻČÜŅŗÖŠµÄCO32-ÓėAlO2-µÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H1£¼0 | B£® | ”÷H2£¾0 | C£® | ”÷H1=”÷H3-2”÷H2 | D£® | 2”÷H4£¾”÷H5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1molČĪŗĪĪļÖŹ¶¼ŗ¬ÓŠ6.02”Į1023øö·Ö×Ó | |
| B£® | ŌŚĻąĶ¬Ģõ¼žĻĀ£¬ĻąĶ¬ĪļÖŹµÄĮæCO”¢N2µÄ»ģŗĻĘųĢåÓėO2µÄ·Ö×ÓøöŹżĻąĶ¬£¬Ō×ÓøöŹżŅ²ĻąĶ¬ | |
| C£® | NaOHµÄĦ¶ūÖŹĮæ40g | |
| D£® | ŌŚ±ź×¼×“æöĻĀ£¬1molO2Óė1molSO3µÄĢå»żĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Ėę×Å“óĘųĪŪČ¾µÄČÕĒ÷ŃĻÖŲ£¬”°½ŚÄܼõÅÅ”±£¬¼õÉŁČ«ĒņĪĀŹŅĘųĢåÅÅ·Å£¬ŃŠ¾æNOx”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮
Ėę×Å“óĘųĪŪČ¾µÄČÕĒ÷ŃĻÖŲ£¬”°½ŚÄܼõÅÅ”±£¬¼õÉŁČ«ĒņĪĀŹŅĘųĢåÅÅ·Å£¬ŃŠ¾æNOx”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ü | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ł¢Ū¢Ż | D£® | ¢Ł¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 ÖÖ | B£® | 2 ÖÖ | C£® | 3 ÖÖ | D£® | 4 ÖÖ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com