
【题目】某Na2CO3样品中含有KCl和NaCl杂质。经分析知含钠31.5%,含氯27.08%(以上均为质量分数),样品中含Na2CO3的质量分数为( )
A.25%
B.50%
C.80%
D.无法确定
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用图所示装置检验乙烯时不需要除杂的是

乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25℃时,0.1 mol/L的氨水。请回答下列问题:
(1)若向0.1 mol·L-1氨水中加入少量硫酸铵固体,此时溶液中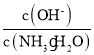 ____(填“增大”“减小”或“不变”)。
____(填“增大”“减小”或“不变”)。
(2)若向0.1mol·L-1氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol·L-1,则
c(SO42-)=_____________。
(3)若向0.1 mol·L-1氨水中加入pH=1的硫酸,且氨水与硫酸的体积比1:1,则所得溶液中各离子物质的量浓度由大到小的顺序是______________。
(4)将足量的AgCl固体分别放入: ①5mL水,②10mL 0.2mol·L-1MgCl2溶液,③20mL 0.5 mol·L-1 NaCI溶液,④40mL 0.1mol·L-1盐酸中溶解至溶液饱和,各溶液中Ag+的物质的量浓度分别为a、b、c、d,它们由大到小的排列顺序是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度为2 mol·L-1的盐酸V L,欲使其浓度变为4 mol·L-1,以下列出的方法中可行的是( )
A. 通入标准状况下的HCl气体44.8 L
B. 将溶液加热蒸发浓缩至0.5V L
C. 蒸发掉0.5V L水
D. 加入10 mol·L-1盐酸0.6V L,再将溶液稀释至2V L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是
A. 0.2mol·L-1Na2SO4溶液中含有Na+和SO42—总物质的量为0.6mol
B. 50mL 2mol·L-1的NaCl溶液和100 mL L 0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等
C. 用1L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1mol·L-1
D. 10g 98%的硫酸(密度为1.84g·cm—3)与10mL 18.4mol·L—1的硫酸的浓度是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配制500mL 3.6mol/L 的稀H2SO4所需18 mol/L的浓H2SO4的体积为________mL。
(2)常温下,将0.1 mol/L的NH4Cl溶液与0.1 mol/L的氨水溶液等体积混合,所得混合液的pH=7,则c(NH4+)=________mol/L,c(Cl-)=________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图为某实验小组依据氧化还原反应(用离子方程式表示)________设计的原电池装置。反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________mol电子。

(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= - 24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= - 47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:__________。
(3)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点_________ (填“升高”还是“降低”),△H______(填“变大”、“变小”或“不变”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.39gNa2O2与CO2完全反应,转移的电子数为NA
B.0.2molNO和0.1molO2混合,所得气体的分子数目为0.2NA
C.84gFe完全转化为Fe3O4,失去的电子数为4NA
D.1molCu和含2molH2SO4的热浓硫酸充分反应,生成SO2分子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、M 为原子序数依次増加的五种短周期元素,A、B、C、D、E 是由这些元素组成的常见化合物,A、B 为厨房中的食用碱,C 是一种无色无味的气体,C、D 都是只有两种元素组成。上述物质之间的转化关系为: ![]() (部分反应物戒生成物省略)。下列说法错误的是
(部分反应物戒生成物省略)。下列说法错误的是
A.原子半径大小序,W>Y>Z>X
B.对应最简单氢化物的沸点:Z>M
C.上述变化过秳中,发生的均为非氧化还原反应
D.Z 和 W 形成的化合物中一定只含离子健
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com