
| A. | 常温常压下,22.4L CO2中含有NA个CO2分子 | |
| B. | 常温下,1L 0.1mol/LNa2S溶液中,含有S2-数为0.1NA | |
| C. | 7.8 g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA | |
| D. | 在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成3 mol Cl2转移的电子数为6NA |
分析 A.常温常压Vm≠22.4L/mol;
B.硫离子为弱酸根离子,溶液中部分硫离子发生水解;
C.根据n=$\frac{m}{M}$并结合过氧化钠与二氧化碳的反应来分析;
D.依据反应中氯元素化合价变化解答.
解答 解:A.常温常压下,气体摩尔体积数值未知,无法计算二氧化碳的物质的量,故A错误;
B.常温下,1L 0.1mol/LNa2S溶液中,含有硫化钠0.1mol,但是硫化钠电离产生的硫离子部分发生水解,所以溶液中的硫离子小于0.1NA,故B错误;
C.7.8g过氧化钠的物质的量n=$\frac{7.8g}{78g/mol}$=0.1mol,而Na2O2与CO2的反应:2Na2O2+2CO2=2Na2CO3+O2↑可知,1molNa2O2参与反应转移1mol电子,故0.1molNa2O2转移0.1mol电子,即0.1NA个,故C正确;
D.在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,氯酸钾中Cl元素化合价由+5价变为0价、HCl中Cl元素化合价由-1价变为0价,每生成3 mol Cl2转移的电子数为5NA,
故D错误;
故选:C.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意标况下气体摩尔体积的使用条件,注意氧化还原反应中化合价变化,题目难度不大.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) | |
| B. | pH=10的Na2A溶液中:2 c(Na+)=c(HA-)+c(H2A)+c(A2-) | |
| C. | 等物质的量浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| D. | 氨水和氯化铵的混合溶液,可能会出现c(NH${\;}_{4}^{+}$)>c(Cl-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2的电子式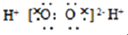 | |
| B. | NH4I的电子式 | |
| C. | 原子核内有8个中子的碳原子:${\;}_{8}^{14}$C | |
| D. | CO2分子的结构式:O=C=O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
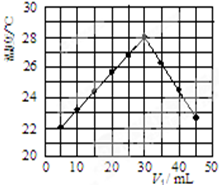 (一)实验方法测定反应热---------中和热测定
(一)实验方法测定反应热---------中和热测定| 实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1Cl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
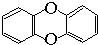 ,其一氯代物有( )
,其一氯代物有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
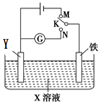 利用如图所示装置进行下列实验,下表中对应叙述正确的是( )
利用如图所示装置进行下列实验,下表中对应叙述正确的是( )| A | X为硫酸氢钠,Y为石墨 K与M连接时;K与N连接时 | 一段时间后溶液的pH均增大 |
| B | X为氯化钠,Y为石墨 K与M连接时; K与N连接时 | 石墨电极反应均为: 4OH--4e-═2H2O+O2↑ |
| C | X为硫酸氢钠,Y为锌 K与M连接时; K与N连接时 | 铁电极反应均为: 2H++2e-═H2↑ |
| D | X为氯化钠,Y为锌 K与M连接时; K与N连接时 | 铁电极的保护方法均为: 牺牲阳极的阴极保护法 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com