
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加。相关信息如下表所示,根据推断回答下列问题(答题时A、B、C、D、E用所对应的元素符号表示)
A | A的一种单质在自然界中硬度最大 |
B | B元素的第一电离能比同周期相邻两个元素都大在同周期中,C元素的最高价氧化物对应的水化物的碱性最强 |
C | D的基态原子M层电子数是K层的2 倍 |
D | E与C位于不同周期,E原子核外最外层电子数与C相同其余各层电子均充满 |
(1)E在周期表中位于第_______周期第 ________族,C基态原子核外电子排布式是_______。
(2)A、B、D三种元素电负性由大到小排列顺序为________,其中A的最高价氯化物为_______(填“极性分子”或“非极性分子”)。
(3)A和B的最简单氢化物中沸点较高的______。原因是__________。
(4)已知:①AH4(g)+2BO2(g)-B2(g)+AO2(g)+2H2O(g)  H1= -867 kJ·mol-1
H1= -867 kJ·mol-1
②2BO2(g)-B2 O4(g)  H2=-56.9 kJ·mol-1写出AH4和B2O4反应的热化学方程式 。
H2=-56.9 kJ·mol-1写出AH4和B2O4反应的热化学方程式 。
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:2014-2015浙江省杭州市下学期高二4月月考化学试卷(解析版) 题型:选择题
下列化学用语正确的是
A.CH4分子的球棍模型: B.乙烯的结构简式:CH2CH2
B.乙烯的结构简式:CH2CH2
C.氯化钠的分子式:NaCl D.K+的结构示意图: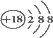
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三4月模拟考试理综化学试卷(解析版) 题型:推断题
选做(12分)【化学——有机化学基础】合成一种有机化合物的途径往往有多种,下图所示为合成醇类物质乙的两种不同途径。
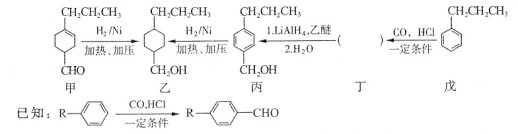
回答下列问题:
(1)甲分子中含氧官能团的名称是 ,由甲催化加氢生成乙的过程中,可能有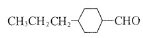 和
和
(写结构简式)生成。
(2)戊的一种属于芳香烃的同分异构体的核磁共振氢谱有两组峰,且峰面积比为3:1,写出戊的这种同分异构体的结构简式 。
(3)由丁 丙的反应类型为 ,检验丙中是否含有丁可选用的试剂是 (填下列各项中序号)。
丙的反应类型为 ,检验丙中是否含有丁可选用的试剂是 (填下列各项中序号)。
a.Na b.NaHCO3溶液 c.银氨溶液 d.浓硫酸
(4)物质乙还可由C10H19Cl与NaOH水溶液共热生成。写出该反应过程中,发生反应的化学方程式并注明反应条件: 。(有机化合物均用结构简式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三第二次模拟化学试卷(解析版) 题型:填空题
(14分)“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题。
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验2条件下平衡常数K= 。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值_______(填具体值或取值范围)。
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时V正 V逆(填“<”,“>”,“=”)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
②2CO(g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(g)= H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:____________
(3)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。常温下,向10 mL 0.01 mol·L-1 H2C2O4溶液中滴加10mL 0.01mol·L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系 ;
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L ,则生成沉淀所需CaCl2溶液的最小浓度为 ________mol/L。
(5)以二甲醚(CH3OCH3)、空气、H2SO4为原料,铂为电极可构成燃料电池,其工作原理与甲烷燃料电池的原理相似。请写出该电池负极上的电极反应式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三第二次模拟化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温下,0.05 mol·L-1Fe2(SO4)3溶液中含Fe3+数目小于0.1 NA
B.30g甲醛中含电子对数为4NA
C.12 g石墨烯(单层石墨)中含有六元环的个数是0.5NA
D.室温下,7.1 g氯气与足量石灰乳充分反应转移电子数小于0.1 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省“江淮十校”高三4月联考理综化学试卷(解析版) 题型:选择题
NA表示阿伙加德罗常数的值。下列判断正确的是
A.常温常压下,17g氨气分子所含质子数为10NA
B.1mol Cl2参加反应,转移电子数一定为2NA.
C.常温常压下,22.4 L C02分子中含有2NA个σ键和2NA个1π键
D.1 L 0. 01 mol.L-1的Na2CO3溶液中含有0.01NA个CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市、石嘴山市高三四月联考理综化学试卷(解析版) 题型:简答题
(13分)废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧黄铜(Cu、Zn合金,含少量杂质Fe)制备胆矾晶体(CuSO4·5H2O)及副产物ZnO。制备流程图如下:
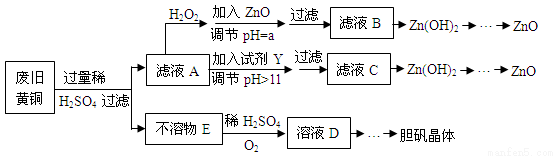
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol/L计算)。
Fe3+ | Fe2+ | Zn2+ | |
开始沉淀的pH | 1.1 | 5.8 | 5.9 |
沉淀完全的pH | 3.0 | 8.8 | 8.9 |
请回答下列问题:
(1)加入ZnO调节pH=a的目的是___________________,a的范围是 。
(2)由不溶物E生成溶液D的化学方程式为______________________________。
(3)滤液A中加入H2O2反应的离子方程式为 。
(4)由溶液D制胆矾晶体包含的主要操作步骤是 。
(5)下列试剂可作为Y试剂的是______。
A.ZnO B.NaOH C.Na2CO3 D.ZnSO4
若在滤液C中逐滴加入盐酸直到过量,则产生的现象是___________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市高三第二次模拟考试化学试卷(解析版) 题型:选择题
臭氧是理想的烟气脱硝剂,其脱硝反应为2NO2(g)+O3(g) N2O5(g)+O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
N2O5(g)+O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 3 | 6 | 12 | 24 |
n(O2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 |
下列有关说法正确的是
A.反应在0~3 s内的平均速率v(NO2)=0.24 mol·L-1·s-1
B.24 s后,若保持其他条件不变,降低温度,达到新平衡时测得c(O2)=0.44 mol·L-1,则反应的ΔH<0
C.在T温度下,起始时向容器中充入1.0 mol NO2、0.5 mol O3和0.50 mol N2O5、0.50 mol O2,反应达到平衡时,压强为起始时的0.88倍
D.在T温度下,起始时向容器中充入2.0 mol N2O5和2.0 mol O2,达到平衡时,N2O5的转化率大于20%
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春市高三质量监测三理综化学试卷(解析版) 题型:实验题
(15分)钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:
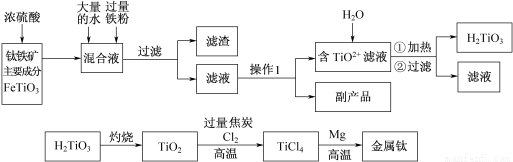
请回答下列问题:
(1)铁在元素周期表中的位置为 。
(2)写出TiO2+水解的离子方程式: 。
加入过量铁粉的作用是:① ;② 。
(3)操作I的实验步骤为:___________________,过滤。
(4)副产品主要成分的化学式为 。
(5)写出TiO2转化成TiCl4的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com